
| A. | SiO2(s)+2C(s)═Si(s)+2CO(g)只能在高温下自发进行,则该反应△H>0 | |
| B. | 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7 | |
| C. | 合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率 | |
| D. | 25℃时,向0.1mol•L-1CH3COOH溶液滴加氨水,c(H+)/c(CH3COOH)增大 |
分析 A.反应自发进行的判断依据是G=△H-T△S<0,反应自发进行;
B.室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,随反应进行醋酸又电离出醋酸根离子和氢离子,溶液显酸性;
C.减小生成物的浓度会使平衡正向移动,减小反应的速率;
D.醋酸溶液中加入氨水发生反应生成醋酸铵,氢离子浓度减小,醋酸分子减小.
解答 解:A.SiO2(s)+2C(s)═Si(s)+2CO(g),反应△S>0,只能在高温下自发进行,依据△H-T△S<0反应自发进行可知,则该反应△H>0,故A正确;
B.室温下,pH=3的CH3COOH溶液中存在电离平衡,与pH=11的NaOH溶液等体积混合,醋酸溶液浓度大于氢氧化钠溶液,随反应进行醋酸又电离出醋酸根离子和氢离子,溶液显酸性,PH<7,故B错误;
C.合成氨生产中将NH3液化分离,降低正反应速率,提高H2的转化率,故C错误;
D.25℃时,向0.1mol•L-1CH3COOH溶液滴加氨水,发生反应CH3COOH+NH3•H2O=CH3COONH4+H2O,$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}CO{O}^{-})}$=$\frac{Ka}{c(C{H}_{3}CO{O}^{-})}$,醋酸根离子浓度增大,比值减小,故D错误;
故选A.
点评 本题考查了反应自发进行的判断依据、弱电解质电离平衡、化学平衡的影响因素,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管未用待测盐酸润洗 | |
| B. | 碱式滴定管未用标准碱液润洗 | |
| C. | 锥形瓶用蒸馏水洗净后未用待测液润洗 | |
| D. | 滴定前仰视读数,滴定后平视读数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量 | 35±15mg/kg |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该气体有毒、无味、密度比空气大 | |
| B. | 将该气体通入紫色石蕊溶液中,石蕊熔液先变红后褪色 | |
| C. | 该气体的性质活泼,它与氢气混合后立即发生爆炸 | |
| D. | 室温下该气体能用钢瓶贮运,所以该气体不与铁反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,负极的电极反应式:Li-e-═Li+ | |
| B. | 充电时,Li0.85NiO2只发生氧化反应 | |
| C. | 该电池不能用水溶液作为电解质 | |
| D. | 放电过程中Li+向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
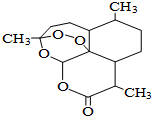 青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物.屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖.青蒿素分子结构如图,下列说法中正确的是( )
青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物.屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖.青蒿素分子结构如图,下列说法中正确的是( )| A. | 青蒿素能与热的NaOH溶液反应 | |
| B. | 青蒿素的分子式为C15H21O5 | |
| C. | 青蒿素分子结构中只含有极性键 | |
| D. | 青蒿素能使酸性KMnO4溶液、溴的CCl4溶液分别褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com