
����Ŀ���������ƣ�NaClO2������Һ�п�����ClO2��HClO2��ClO2����Cl���ȣ�����HClO2��ClO2������Ư�����ã���ClO2���ж����塣ij�¶��£����ֺ�����ֺ�����pH�仯�����ͼ��ʾ������˵������ȷ����
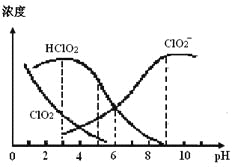
A. ʹ�ø�Ư��������pHԼΪ5.0
B. ���¶���NaClO2��Һ�У�c(Na��)��c(ClO2��)��c(OH��)��c(H��)
C. ���¶���HClO2�ĵ���ƽ�ⳣ������ֵKa��1.0��10��6
D. ��ͬpH��NaClO2��Һ�д������й�ϵ��c(Na��)= c(ClO2��)+ c(HClO2)+ c(ClO2)

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������²��ϼ�3D��ӡ��������ѧ�����Ƴ�һ���������ռ��ܽ������ŷŵ�CO2�Ը��Ӱ�ȫ�����ۺ�Ч�ķ�ʽ�����������������ڲ�����Na2CO3��Һ����ԭ����ͼ��ʾ��

��1��������������CO2��ԭ����_____________(�����ӷ���ʽ����)���˹�����_______�����������������ų����������Ĺ��̡�
��2�������չ����й��ڽ�������Һ����˵����ȷ����_____________��
a.����ǰ��Һ��c(Na��)>c(CO32��)>c(HCO3��)>c(OH��)>c(H��)
b.���չ����У���ϵ�����еĺ�̼����CO32����HCO3����H2CO3
c.��n(CO2)��n(Na2CO3)��1:3ʱ����Һ��c(CO32��)<c(HCO3��)
d.��Һ��ʼ����c(Na��)��c(H��)��2c(CO32��)��c(HCO3��)��c(OH��)
��3�������յ�CO2��������Ƶ���ϩ��
��֪��2CO2(g)��6H2(g) ![]() C2H4(g)��4H2O(g)��H����127.8 kJ/mol����ͼ����a��ʾ�����Ϊ2 L�ĺ��������У�Ͷ��Ϊ1 mol CO2��3 mol H2ʱ������¶ȶ�CO2��ƽ��ת���ʵ�Ӱ�죬�ı�Ͷ�ϱȲ�����õ�����b��
C2H4(g)��4H2O(g)��H����127.8 kJ/mol����ͼ����a��ʾ�����Ϊ2 L�ĺ��������У�Ͷ��Ϊ1 mol CO2��3 mol H2ʱ������¶ȶ�CO2��ƽ��ת���ʵ�Ӱ�죬�ı�Ͷ�ϱȲ�����õ�����b��

�ٸ�������a����250��ʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��K��_____________��������ֵ�г�����ʽ���ɣ�
��b������Ͷ�ϱ�n(H2)/n(CO2)______3�������������������������������ж�������____________________________
������˵����ȷ����_____________��
a.ƽ�ⳣ����С��M=M1> N
b.�����������䣬b����ʱ���Ӵ�����������250��ʱCO2��ƽ��ת���ʿ��ܴﵽM
c.��ѹǿ�����������ܶȻ�n(H2)/n(CO2)����ʱ������Ϊ��ѧ��Ӧ�Ѵﵽƽ��״̬
d.��ҵ�����в�ȡ�ϸ��¶ȣ�250 �����ң���Ϊ����ߴ������Լӿ췴Ӧ���ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ӵ�ص�Ӧ�úܹ㣬���������Ͽ��������á�ij����ӵ����������������ﮣ�LiCoO2�����������Ȳ�ں������ȡ����ʱ��������ӵ�ظ��������ķ�ӦΪ6C+xLi++xe- = LixC6�������������¹������̻������������е�ijЩ������Դ����������δ��������

�ش��������⣺
��1��LiCoO2�У�CoԪ�صĻ��ϼ�Ϊ ��
��2��д��������������з�����Ӧ�����ӷ���ʽ ��
��3���������һ����80���½��У�д���ò����з���������������ԭ��Ӧ�Ļ�ѧ����ʽ �������������H2SO4��H2O2�Ļ��Һ����ȱ���� ��
��4��д���������������з�����Ӧ�Ļ�ѧ����ʽ ��
��5����ŵ�����У�����LiCoO2��Li1-xCoO2֮���ת����д���ŵ�ʱ��ط�Ӧ����ʽ ��
��6�����������У����ŵ紦������������������Ļ��գ���ԭ���� �����������չ����У��ɻ��յ��Ľ����������� ���ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ���ǣ� ��
A.��0.1mol��L-1CH3COOH��Һ�м�������ˮ����Һ��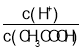 ��С
��С
B.��CH3COONa��Һ��20��������30�棬��Һ��![]() ����
����
C.��pH=8��NaB��Һ�У�c(Na+)-c(B-)=9.9��10-8mol��L-1
D.��AgCl��AgBr�ı�����Һ�м�������AgNO3����Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼����������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
(1) ����ȼ�շų��������ȣ�����Ϊ��Դ������������������
��֪����2CH4��g��+3O2��g��=2CO��g��+4H2O��l����H1=-1214kJ/mol
��2CO(g)+O2(g)=2CO2(g) ��H2=-566 kJ/mol
���ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ____________________________________��
(2) ������ʯī�缫����KOH��Һ�У��������ֱ�ͨ��CH4��O2�����ɼ���ȼ�ϵ�ء��为���缫��Ӧʽ�ǣ�_____________________________��
��3��ijͬѧ���ü���ȼ�ϵ�������һ�ֵ�ⷨ��ȡFe(OH)2��ʵ��װ�ã�����ͼ��ʾ����ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ������˵������ȷ����______������ţ�
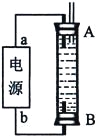
A����Դ�е�aһ��Ϊ������bһ��Ϊ����
B��������NaCl��Һ��Ϊ���Һ
C��A��B���˶������������缫
D�����������ķ�Ӧ�ǣ�2H++ 2e��= H2��
��4������ͬ����CO��g����H2O��g���ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У����з�Ӧ��
CO��g��+H2O��g��===CO2��g��+H2��g�����õ������������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | |
H2O | CO | CO2 | |||
1 | 650 | 2 | 4 | 1.6 | 5 |
2 | 900 | 1 | 2 | 0.4 | 3 |
3 | 900 | 1 | 2 | 0.4 | 1 |
��ʵ��
��ʵ��3��ʵ��2��ȣ��ı������������_________________����һ��������ɣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л������ﷴӦ����ͼ���ݴ˻ش��������⣺

��1����ϩ�ĽṹʽΪ��__________��
��2��д����Ӧ�ڢۢܵĻ�ѧ����ʽ��
��_________________________����Ӧ���ͣ�___________��
��_________________________����Ӧ���ͣ�___________��
��_________________________����Ӧ���ͣ�___________��
��3��ʵ���ҳ�������װ����ȡ������������ش�������⣺

��Ũ�����������_______________��
�ڱ���̼������Һ����Ҫ������___________________��
����Ҫ���Ƶõ������������������Ӧ���õIJ�����_________��
�ܽ��и�ʵ��ʱ��������Թܼ��м��뼸�����Ƭ����Ŀ����_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���������ȷ����
A. 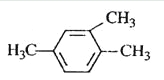 1,3,4-���ױ�
1,3,4-���ױ�
B. 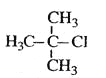 2-��-2-�ȱ���
2-��-2-�ȱ���
C. 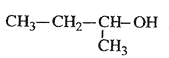 2-��-1-����
2-��-1-����
D. 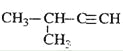 2-��-3-��Ȳ
2-��-3-��Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��� 0.1000 mol��L![]() NaOH��Һ�ζ� 20.00mL0.1000 mol��L
NaOH��Һ�ζ� 20.00mL0.1000 mol��L![]()
![]() ��Һ���õζ�������ͼ������˵����ȷ����
��Һ���õζ�������ͼ������˵����ȷ����

A.�����ʾ��Һ�У�![]()
B.�����ʾ��Һ�У�![]()
C.�����ʾ��Һ�У�![]()
D.�ζ������п��ܳ��֣�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ʽ��NaHY��ˮ��Һ�Լ��ԣ�����������ȷ���ǣ� ��
A.H2Y�ĵ��뷽��ʽΪ��H2Y![]() 2H����Y2��
2H����Y2��
B.HY����ˮ�ⷽ��ʽΪ��HY����H2O![]() H3O����Y2��
H3O����Y2��
C.����ʽ����Һ������Ũ�ȹ�ϵΪ��c(Na��)��c(HY��)��c(OH��)��c(H��)��c(Y2��)
D.����ʽ����Һ������Ũ�ȹ�ϵΪ��c(Na��)��c(Y2��)��c(HY��)��c(OH��)��c(H��)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com