
| A.用酒精萃取碘水中的碘 |
| B.用蒸馏的方法将自来水制成蒸馏水 |
| C.用溶解、过滤的方法分离硝酸钾和沙子 |
| D.用加热的方法分离氯化钠和氯化铵固体 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:多选题
| A.福尔马林(甲酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 |
| B.溴乙烷(乙醇):多次加水振荡,分液,弃水层 |
| C.苯(苯酚):加溴水,振荡,过滤除去沉淀 |
| D.乙酸乙酯(乙酸):加氢氧化钠溶液,充分振荡,分液,弃水层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在除去生石灰中的石灰石时,加水后进行过滤 |
| B.用过滤的方法除去碘水中的碘 |
| C.用乙醇萃取碘水中的碘 |
| D.用溶解过滤蒸发的方法除去固体BaCl2中的BaSO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 物质 | 所含杂质 | 所用试剂 | 方法 | |
| A | O2 | CO2 | NaOH溶液 | 洗气 |
| B | FeSO4 | CuSO4 | Fe | 过滤 |
| C | 酒精 | 水 | CaO | 蒸发 |
| D | KCl | K2CO3 | 盐酸溶液 | 蒸发 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A. 除去混有的杂质气体 |
B. 浓硫酸稀释 |
C.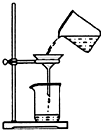 分离出AgNO3溶液中的AgCl |
D. 称量30.46g的NaOH固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除去Al中的少量Fe:加入足量的盐酸,过滤 |
| B.除去CO2中的少量HCl:通入Na2SO3溶液,收集气体 |
| C.除去FeCl2溶液中的少量FeCl3:加入足量铜粉,充分反应后,过滤 |
| D.除去KCl溶液中的少量MgCl2:加入适量的KOH溶液,过滤后加入少量稀盐酸,加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
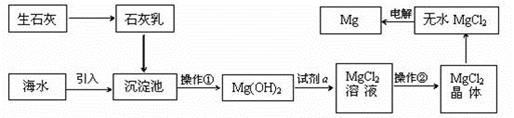
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com