
KIČÜŅŗŌŚĖįŠŌĢõ¼žĻĀÄÜÓėŃõĘų·“Ó¦”£ĻÖÓŠŅŌĻĀŹµŃé¼ĒĀ¼£ŗ
ŹµŃ鱹ŗÅ | ¢Ł | ¢Ś | ¢Ū | ¢Ü | ¢Ż |
ĪĀ¶Č(”ę) | 30 | 40 | 50 | 60 | 70 |
ĻŌÉ«Ź±¼ä(s) | 160 | 80 | 40 | 20 | 10 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________________________£»
£Ø2£©øĆŹµŃéµÄÄæµÄŹĒ____________________________£»
£Ø3£©ŹµŃéŹŌ¼Į³żĮĖ1mol/L KIČÜŅŗ”¢0.1mol/L H2SO4ČÜŅŗĶā£¬»¹ŠčŅŖµÄŹŌ¼ĮŹĒ____________£¬ŹµŃéĻÖĻóĪŖ____________________________£»
£Ø4£©ÉĻŹöŹµŃé²Ł×÷ÖŠ³żĮĖŠčŅŖ£Ø3£©µÄĢõ¼žĶā£¬»¹±ŲŠėæŲÖĘ²»±äµÄŹĒ________(Ģī×ÖÄø)£®
A£®ĪĀ¶Č B£®ŹŌ¼ĮµÄÅØ¶Č C£®ŹŌ¼ĮµÄÓĆĮæ(Ģå»ż) D£®ŹŌ¼ĮĢķ¼ÓµÄĖ³Šņ
£Ø5£©ÓÉÉĻŹöŹµŃé¼ĒĀ¼æÉµĆ³öµÄ½įĀŪŹĒ____________________________£»
£Ø6£©ČōŅŖ½ųŠŠĖįŠŌ¶Ō·“Ó¦ĖŁĀŹµÄÓ°ĻģµÄĢ½¾æŹµŃ飬Äć»į²ÉČ”µÄ“ėŹ©ŹĒ____________________________£»
 ŠĀæĪ±źĶ¬²½ŃµĮ·ĻµĮŠ“š°ø
ŠĀæĪ±źĶ¬²½ŃµĮ·ĻµĮŠ“š°ø Ņ»ĻßĆūŹ¦æŚĖćÓ¦ÓĆĢāĢģĢģĮ·Ņ»±¾Č«ĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦æŚĖćÓ¦ÓĆĢāĢģĢģĮ·Ņ»±¾Č«ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĖÄ“ØŹ”ø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Cu2OæÉÓɵē½āÖĘČ”£¬ČēĶ¼ĖłŹ¾£¬µē½ā×Ü·“Ó¦£ŗ2Cu+H2O=Cu2O+H2”ü”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
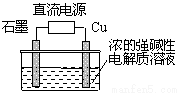
 A£®ŹÆÄ«µē¼«ÉĻ²śÉśĒāĘų
A£®ŹÆÄ«µē¼«ÉĻ²śÉśĒāĘų
 B£®Ķµē¼«·¢Éś»¹Ō·“Ó¦
B£®Ķµē¼«·¢Éś»¹Ō·“Ó¦
 C£®Ķµē¼«½ÓÖ±Į÷µēŌ“µÄøŗ¼«
C£®Ķµē¼«½ÓÖ±Į÷µēŌ“µÄøŗ¼«
 D£®øĆ·“Ó¦Ņ²æÉÉč¼ĘĪŖŌµē³Ų
D£®øĆ·“Ó¦Ņ²æÉÉč¼ĘĪŖŌµē³Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğČĆɹÅŗ¼½õŗóĘģ·Ü¶·ÖŠŃ§øßŅ»ĻĀĘŚÖŠ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
×īŠĀŃŠ¾æ±ķĆ÷£ŗNOĪüŹÕÖĪĮĘ·ØæÉæģĖŁøÄÉĘSARSÖŲÖ¢»¼ÕßµÄȱŃõדæö£¬»ŗ½ā²”Ē锣²”¶¾Ń§ŃŠ¾æĶ¬Ź±Ö¤Źµ£¬NO¶ŌSARS²”¶¾ÓŠÖ±½ÓŅÖÖĘ×÷ÓĆ”£ĻĀĮŠ¹ŲÓŚNOµÄŠšŹöÕżČ·µÄŹĒ( )
A£®NOŹĒŅ»ÖÖŗģ×ŲÉ«µÄĘųĢå
B£®³£ĪĀ³£Ń¹ĻĀ£¬NO²»ÄÜÓėæÕĘųÖŠµÄŃõĘųÖ±½Ó»ÆŗĻ
C£®ŗ¬µČÖŹĮæµÄŃõŌŖĖŲµÄNOŗĶCOµÄĪļÖŹµÄĮæĻąµČ
D£®NOŅ×ČÜÓŚĖ®£¬²»ÄÜÓĆÅÅĖ®·ØŹÕ¼Æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶ž5ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĶ¼±ķŹ¾Ä³øß·Ö×Ó»ÆŗĻĪļµÄ½į¹¹Ę¬¶Ļ£¬¹ŲÓŚøĆøß·Ö×Ó»ÆŗĻĪļµÄĶʶĻÕżČ·µÄŹĒ( )
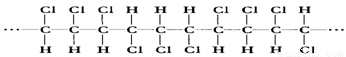
A£®øĆøß·Ö×ÓŹĒ¾ÓÉĖõ¾Ū·“Ó¦µĆµ½
B£®øĆøß·Ö×ӵķÖ×ÓŹ½ŹĒ(C3H3Cl3)n
C£®¾ŪŗĻĪļµÄµ„ĢåŹĒCHCl£½CHClCH3
D£®ČōnĪŖ¾ŪŗĻ¶Č£¬ŌņĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ97n
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”ø߶ž5ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃéÄÜ»ńµĆ³É¹¦µÄŹĒ( )
A£®ÖĘČ”äå±½£ŗĢśŠ¼”¢äåĖ®”¢±½
B£®ŅŖ¼ģŃéĀ±“śĢžÖŠµÄĀ±ĖŲŌ×Ó£¬æÉĻņĘäČÜŅŗÖŠ¼ÓČėAgNO3ČÜŅŗ
C£®±½·ÓÓŠĖįŠŌ£¬æÉŹ¹×ĻÉ«ŹÆČļ±äŗģ
D£®ÓĆäåĖ®æɼų±š±½”¢CCl4”¢±½ŅŅĻ©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ°²»ÕŹ¦“óø½ÖŠø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
æÉÄę·“Ó¦2SO2(g)+O2 (g) 2SO3 (g)£¬øł¾ŻĻĀ±ķÖŠµÄŹż¾ŻÅŠ¶ĻĻĀĮŠĶ¼Ļń“ķĪóµÄŹĒ
2SO3 (g)£¬øł¾ŻĻĀ±ķÖŠµÄŹż¾ŻÅŠ¶ĻĻĀĮŠĶ¼Ļń“ķĪóµÄŹĒ

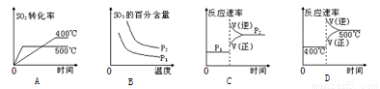
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ°²»ÕŹ¦“óø½ÖŠø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·ØæɱķŹ¾·½·ØÕżČ·µÄŹĒ
A£®½«0.5molN2ŗĶ1.5molH2³äČėŅ»ĆܱÕČŻĘ÷ÖŠ³ä·Ö·“Ó¦£¬·Å³öČČĮæ19.6kJŌņøĆČČ»Æѧ·½³ĢŹ½ĪŖN2(g)+3H2(g) 2NH3(g) ”÷H=-39.2kJ•mol-1
2NH3(g) ”÷H=-39.2kJ•mol-1
B£®ÓÉC(ŹÆÄ«)=C(½šøÕŹÆ)£»”÷H=+1.9kJ•mol-1£¬æÉÖŖ½šøÕŹÆ±ČŹÆÄ«ĪȶØ
C£®ŌŚĻ”ČÜŅŗÖŠ£ŗH++OH-ØTH2O”÷H=-57.3kJ/mol£¬Čō½«ŗ¬40.0gNaOHµÄĻ”ČÜŅŗÓėĻ”“×ĖįĶźČ«ÖŠŗĶ£¬·Å³öµÄČČĮæŠ”ÓŚ57.3kJ
D£®ŌŚ101kPaŹ±£¬2gH2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö285.8kJČČĮ棬ĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ£ŗ2H2(g)+O2(g)ØT2H2O(l)”÷H= -285.8kJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”øßŅ»ĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŃŠ¾æµē»ÆѧøÆŹ“¼°·Ą»¤µÄ×°ÖĆČēĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲĖµ·Ø“ķĪóµÄŹĒ

A£®dĪŖŹÆÄ«£¬ĢśĘ¬øÆŹ“¼Óæģ
B£®dĪŖŹÆÄ«£¬ŹÆÄ«ÉĻµē¼«·“Ó¦ĪŖ£ŗO2 + 2H2O + 4e £½ 4OHØC
C£®dĪŖŠææ飬ĢśĘ¬²»Ņ×±»øÆŹ“
D£®dĪŖŠææ飬ĢśĘ¬ÉĻµē¼«·“Ó¦ĪŖ£ŗ2H+ + 2e £½ H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğÕć½Ź”ø߶žĻĀĘŚÖŠ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÉčNAĪŖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£® 0£®1mol Na2O2Óė×ćĮæµÄ³±ŹŖµÄ¶žŃõ»ÆĢ¼·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0£®1NA
B£® 1molĆ¾Óė×ćĮæO2»ņN2·“Ӧɜ³ÉMgO»ņMg3N2Ź§Č„µē×Ó·Ö±šĪŖ2NAŗĶ3NA
C£® ŗ¬NAøöNa+µÄNa2O2ČÜÓŚ1LĖ®ÖŠ£¬Na+µÄĪļÖŹµÄĮæÅضČĪŖ1 mol/L
D£® ijĆܱÕČŻĘ÷ÖŠŹ¢ÓŠ0£®2molN2ŗĶ0£®3molH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦£¬×ŖŅʵē×ӵďżÄæĪŖ0£®6 NA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com