
【题目】遇碘水显蓝色的是
A. 羊肉 B. 鲜鱼片 C. 面粉 D. 鸡蛋
科目:高中化学 来源: 题型:
【题目】如图所示,一密闭容器被无摩擦、可滑动的两隔板A、B分成甲、乙两室。标准状况下,在乙室充入8.4g N2,甲室充入8.8g H2和O2的混合气体。

(1)甲室中的原子个数约为 ______________个,H2与O2的质量比为_____________。
(2)维持温度不变,将隔板A固定在“3”处,将隔板B固定在“5”处,此时甲、乙两室中气体的压强比P(甲):P(乙)=______________。
(3)用电火花处理甲室中的气体使其充分反应,反应后恢复至标准状况。甲室与乙室此时的体积比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.现有下列粒子:①BF3、②HCN、③NH2- 请填写下列空白(填序号):
(1)存在极性键的非极性分子是__________;
(2)中心原子轨道为sp3杂化的是________;
(3)只存在σ键的微粒是__________, 存在π键的微粒是__________,
(4)空间构型呈“V”形的是__________。
Ⅱ.氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于 NH4+的性质。
(1)N2H62+在碱性溶液中反应的离子方程式:_______________,
(2)NH2-的电子式为__________________________,
(3)写出二种与N3-等电子体的微粒化学式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含钴催化剂废料(含Fe3O4、Co2O3、Al2O3、CaO及SiO2为原料制取Co3O4的一种工艺流程如下:
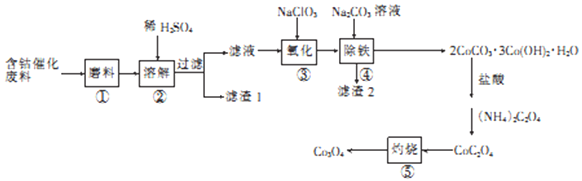
回答下列问题:
(1)CoC2O4中Co的化合价为_____。
(2)步骤②经溶解后过滤,滤渣1的主要成分为____(填化学式),滤液中含有_____种阳离子。
(3)步骤③氧化对Fe2+全部转化为Fe3+,反应的离子方程式为_______,检验其是否已完全氧化自方法是______________。
(4)步骤国加Na2CO3溶液的目的是_____________,滤渣2中含有Na2Fe6(S04)4(OH)x,则x=____,滤渣2中__________(填“含有”或“不含”Al(OH)3。
(5)某工厂用m1kg含钴催化剂废料Co2O3的质量分数为35%)制备Co3O4,最终得到产品m2kg,其产率为________(列出算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应:2NO(g)+O2(g)![]() 2NO2(g),体系中n(NO2)随时间的变化如表:
2NO2(g),体系中n(NO2)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)(mol) | 0.00 | 0.010 | 0.012 | 0.013 | 0.013 | 0.013 |
(1)写出该反应的平衡常数表达式:K=____________。已知:K(350℃)300℃),则该反应是________(填吸或放)热反应。
(2)下图中表示NO的变化的曲线是_________(填字母)用O2表示从0~2 s内该反应的平均速率v=_________。
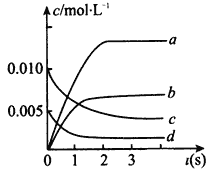
(3)能说明该反应已达到平衡状态的是______________(填字母)
A.c(NO2)=2c(O2) B.容器内压强保持不变
C.v逆 (NO)=2v正(O2) D.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚对苯二甲酸乙二醇酯(PET)俗称涤纶,是一种重要的有机高分子材料。其结构为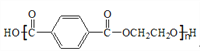 。其合成路线如下图:
。其合成路线如下图:
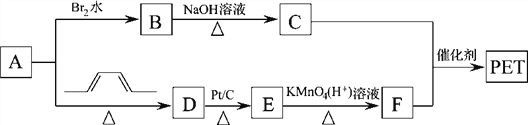
已知:![]()
回答下列问题:
(1)B的名称是_________________,C中官能团的名称是________________________。
(2)A→D的反应类型为________________________________。
(3)E的结构简式为____________________。
(4)写出C+F→PET的化学反应方程式______________________________。
(5)G是F的同系物,其相对分子质量比F多14,则符合该条件的G的结构共有_________种,写出其中苯环上只有一个取代基的结构简式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镓(Ga)位于周期表的第四周期,与Al同主族,主要存在Ga3+、GaO2-两种离子形态,被广泛应用于电子工业。
(1)Ga的原子序数为______。
(2)半导体材料氮化稼是由Ga与NH3在一定条件下合成的,该过程中每生成3molH2时,就会放出30.8kJ的热量。
①反应的热化学方程式是________。
②反应的化学平衡翻常数表决达式是_________________。
③在恒温恒容的密闭体系内进行上述可逆反应,下列有关表达正确的是_____(填字母代号).

A.Ⅰ图象中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压
B.Ⅱ图象中纵坐标可以为稼的转化率
C.Ⅲ图象中纵坐标可以为化学反应速率
D.Ⅳ图象中纵坐标可以为体系内混合气体的平均相对分子质量
(3)工业上多用电解精炼法提纯稼。具体原理如下图所示:

已知:金属的活动性Zn>Ga>Fe>Cu
①X为电源的_____极,电解精炼稼时阳极泥的成分是__________;
②在电解过程中使某种离子迁移到达阴极并在阴极放电析出高纯稼, 请写出该电解过程中的电极反应方程式:阳极_________;阴极_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作错误的是
A. 用药匙取用少量Na2SO4固体
B. 用胶头滴管滴加少量NaCl溶液
C. 用酒精灯直接加热试管、蒸发皿
D. 用10mL量筒量取8.50mL1.0 mol·L-1NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com