
实验题
如图所示,将浸透了石蜡油的石棉放在硬质玻璃试管的底部,试管中放了碎瓷片,加热.
(■图片上文字不清晰)
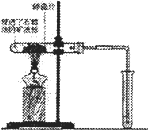
(1)实验装置中矿渣棉的作用是________________________,碎瓷片的作用是________________________.
(2)反应生产的气体使小试管中的酸性高锰酸钾溶液________.
(3)假设石蜡油中的某种烃的化学式C18H38,它发生裂化反应生成了两种烃,其中的一种为辛烷,另一种为烃A,则烃A的化学式为________,若辛烷又发生裂化反应生成丁烷和烃B,则烃B的化学式为________,丁烷又发生裂化反应生成了乙烷和烃C,则烃C与溴押氯化碳溶液反应的化学方程式为________.
科目:高中化学 来源: 题型:
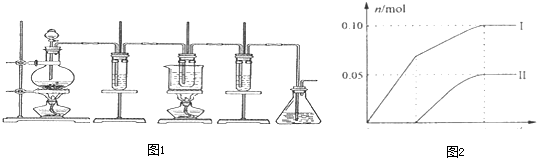
 某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).回答下列问题:
某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).回答下列问题:| 100Q |
| 3 |
| 100Q |
| 3 |
| 100Q |
| 3 |
| 100Q |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O
查看答案和解析>>
科目:高中化学 来源:2012-2013学年黑龙江省哈尔滨九中高三第三次月考化学试卷(解析版) 题型:解答题
 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com