
 某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.
某兴趣小组利用文献资料设计方案对氯及其化合物进行探究.| 烧杯编号 | 1 | 2 | 3 | 4 |
| 氯酸钾饱和溶液 | 1mL | 1mL | 1mL | 1mL |
| 氯化钾固体 | 1g | 1g | 1g | 1g |
| 水 | 8mL | 6mL | 3mL | 0mL |
| 硫酸(6mol/L) | 0mL | 2mL | (5)mL | 8mL |
| 现象 | 无现象 | 溶液呈浅黄色 | 溶液呈黄绿色,生成浅黄绿色气体 | 溶液呈黄绿色, 生成黄绿色气体 |
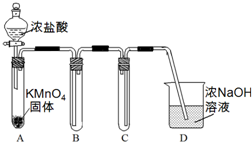
分析 Ⅰ(1)用高锰酸钾和浓盐酸反应制取氯气,氯气的密度比空气大,收集时采用长进短出的方式,C是安全装置;
(2)新制的饱和氯水中存在H2O,Cl2,HClO分子,存在H+,OH-,Cl-,ClO-离子;
(3)①氯水中存在平衡:Cl2+H2O?HCl+HClO,加入石灰石后,HCl与CaCO3反应浓度减小,使平衡向右移动,HClO浓度增大,漂白效果好;
②氯水中含盐酸、次氯酸,加入石灰石后,HCl与CaCO3反应,据此解答;
Ⅱ(4)①从表中数据看出其他条件相同时,溶液的总体积相同,只有硫酸的浓度不同,得出本实验的目的;
②根据每组实验的总体积应相同计算出烧杯3取用硫酸的体积;
(5)根据物质沸点不同设计实验.
解答 解:Ⅰ(1)用高锰酸钾和浓盐酸反应制取氯气,氯气的密度比空气大,收集时采用B装置长进短出的方式,C是安全装置,防止D中的溶液进入B,
故答案为:收集氯气;防止D中的溶液进入B;
(2)新制的饱和氯水中存在H2O,Cl2,HClO分子,存在H+,OH-,Cl-,ClO-离子,含氯元素的微粒有:Cl-、Cl2、ClO-、HClO,
故答案为:Cl-、Cl2、ClO-、HClO;
(3)①氯水中存在平衡:Cl2+H2O?HCl+HClO,加入石灰石后,HCl与CaCO3反应浓度减小,使平衡向右移动,HClO浓度增大,漂白效果好,
故答案为:氯水中存在平衡:Cl2+H2O?HClO+HCl,CaCO3与盐酸反应使平衡正移,增大HClO的浓度,漂白效果增强;
②氯水中含盐酸、次氯酸,加入石灰石后,HCl与CaCO3反应生成氯化钙、二氧化碳和水,总反应方程式为:CaCO3+2Cl2+H2O═2 HC1O+CO2+CaCl2,
故答案为:CaCO3+2Cl2+H2O═2HC1O+CO2+CaCl2;
Ⅱ(4)①从表中数据看出其他条件相同时,溶液的总体积相同,只有氢离子的浓度不同,得出本实验的目的为:其他条件相同时,氢离子浓度不同对化学反应速率的影响,
故答案为:其他条件相同时,氢离子浓度不同对化学反应速率的影响;
②根据每组实验的总体积应相同计算出烧杯3取用硫酸的体积,实验1的总体积为1mL+8mL+0mL=9mL,所以烧杯3中硫酸的体积为:9mL-1mL-3mL=5mL,
故答案为:5;
(5)根据ClO2沸点为10℃,熔点为-59℃,液体为红色,Cl2沸点为-34℃,液态为黄绿色,为验证Cl2中含有ClO2,收集一试管气体,盖上胶塞,放入冰水混合物中,观察液体(或气体)颜色变化,若出现红色,则说明Cl2中含有ClO2,
故答案为:收集一试管气体,盖上胶塞,放入冰水混合物中,观察液体(或气体)颜色变化.
点评 本题考查了实验室制氯气的方法,氯水的成分,化学平衡移动原理的应用,浓度对化学反应速率影响的探究,重点是实验能力的考查,难度适中,注意阐述的准确性.


科目:高中化学 来源: 题型:选择题
| A. | 都具有强氧化性 | |
| B. | 在常温下都能与铜反应 | |
| C. | 露置于空气中都能形成白雾 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
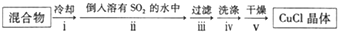
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
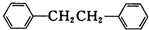 )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为: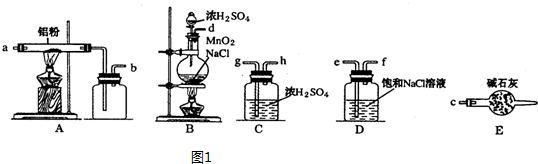
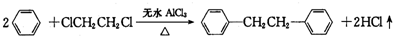
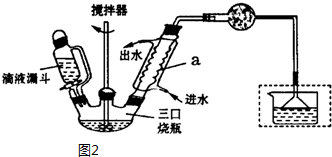
| 名称 | 相对分子质量 | 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
| 1,2一二氯乙烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
| 无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水水解,微溶苯 |
| 联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
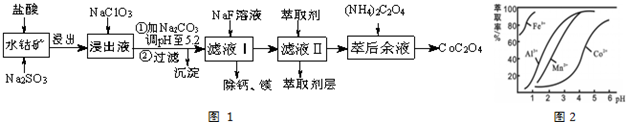
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
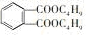 ),过量摄入塑化剂会对肝肾功能造成影响,甚至诱发癌症.下列有关说法正确的是( )
),过量摄入塑化剂会对肝肾功能造成影响,甚至诱发癌症.下列有关说法正确的是( )| A. | DBP的分子式为C16H22O4 | |
| B. | 1mol DBP可以与5molH2反应 | |
| C. | 1mol DBP在碱性条件下水解时消耗4molNaOH | |
| D. | DBP所有原子在同一平面内 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com