
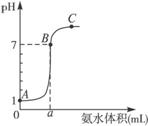
A.盐酸的浓度为1 mol/L
B.在B点:c(![]() )=c(Cl-)>c(OH-)=c(H+),且a>10
)=c(Cl-)>c(OH-)=c(H+),且a>10
C.在A、B间任意一点:c(Cl-)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.在C点:c(![]() )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
科目:高中化学 来源: 题型:058
向25 mL某浓度的稀盐酸中逐滴滴入0.20 mol·L-1NaOH溶液,用酚酞作指示剂,以测该盐酸的物质的量浓度.滴定后计算知该稀酸浓度为0.10 mol·L-1.
(1)在下面实验通知单中,写出所需仪器名称、数量以及玻璃仪器规格.
化学实验通知单(部分内容)
|
药品或仪器 |
数量 |
规格 |
|
铁架台(带滴定管夹) |
|
|
|
酸式滴定管 |
|
|
|
碱式滴定管 |
|
|
|
锥形瓶 |
|
|
(2)在下图中画出滴定过程中,pH随滴入NaOH(标况)体积V的变化曲线,假设V体积由0 mL逐渐滴至20 mL.(已知lg3=0.5)

查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:058
(1)在下面实验通知单中,写出所需仪器名称、数量以及玻璃仪器规格.
化学实验通知单(部分内容)
|
药品或仪器 |
数量 |
规格 |
|
铁架台(带滴定管夹) |
|
|
|
酸式滴定管 |
|
|
|
碱式滴定管 |
|
|
|
锥形瓶 |
|
|
(2)在下图中画出滴定过程中,pH随滴入NaOH(标况)体积V的变化曲线,假设V体积由0 mL逐渐滴至20 mL.(已知lg3=0.5)

查看答案和解析>>
科目:高中化学 来源: 题型:

(1)H2SO4溶液物质的量浓度为____________;
(2)若a=2.3,则用于沉淀Fe3+而消耗NaOH的体积是__________mL,铝土矿中各组成成分的质量分数:Al2O3为__________,Fe2O3为__________,SiO2为__________;
(3)a值的范围应是__________,在这个范围内,a值越大,__________的质量分数越小.
查看答案和解析>>
科目:高中化学 来源: 题型:

求:(1)H2SO4溶液的物质的量浓度是多少?
(2)若A=2.3 mL,铝土矿中Al2O3的质量分数是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com