
一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如2Fe3+ + Cu ==2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e- ==Cu2+,还原反应式:2Fe3+ + 2e- ="=" 2Fe2+。并由此实现了化学能与电能的相互转化。据此,回答下列问题:
(1)将反应Zn + 2H+ = Zn2+ + H2↑拆写为两个“半反应式”:其中,氧化反应为: 。
(2)由题(1)反应,设计成原电池如图所示:
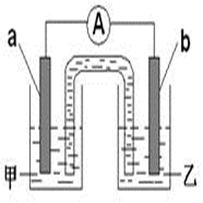
若电极a为Zn ,电极b可选择材料: (只填一种);电解质溶液甲是 ;电极b处的电极反应式: 。
(3)由反应2H2 + O2 2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
2H2O ,设计出以稀硫酸为电解质溶液的燃料电池,其电极反应式为:负极 ,正极 。
(1)Zn-2e-= Zn2+(2分)
(2)Cu(合理给1分),ZnSO4(1分),2H+ + 2e- = H2↑(2分).
(3)负极:2H2 - 4e- = 4H+ ,正极:O2 + 4H+ + 4e- = 2H2O(4分)
【解析】
试题分析:(1)依据题意,由2Fe3+ + Cu ==2Fe2++Cu2+,可拆写为氧化反应式:Cu-2e- ==Cu2+,还原反应式:2Fe3+ + 2e-==2Fe2+ ,可得:反应Zn + 2H+ = Zn2+ + H2↑拆写为两个“半反应式”,氧化反应为Zn失去2e-生成Zn2+,故氧化反应式为:Zn-2e-= Zn2+;
(2)如图,组成的原电池中若电极a为Zn ,则电解质溶液应为ZnSO4 ,电极b选择材料的化学性质应比锌不活泼,可为Cu或C,则电解质溶液已为稀H2SO4,故电极b处的电极反应式为:2H+ + 2e- = H2↑
(3)根据反应2H2 + O2 2H2O ,以稀硫酸为电解质溶液设计的燃料电池,其中负极的电极反应式为:2H2 - 4e- = 4H+ ,正极的电极反应式为:O2 + 4H+ + 4e- = 2H2O;
2H2O ,以稀硫酸为电解质溶液设计的燃料电池,其中负极的电极反应式为:2H2 - 4e- = 4H+ ,正极的电极反应式为:O2 + 4H+ + 4e- = 2H2O;
考点:氧化还原反应、化学电池
点评:该题是中等难度的试题,也是高考中的常见考点。试题注重基础,侧重能力的训练。该题的关键是明确原电池的工作原理,然后结合同样灵活运用、分析、判断即可。


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
已知硝酸与金属反应时,在不同条件下,硝酸有不同的还原产物,甚至在同一反应中可同时得到多种还原产物。现有HNO3、NH4NO3、N2O、H2O、Zn、Zn(NO3)2六种物质,可以利用其中五种物质组成一个完整的化学反应,也可以用六种物质组成一个完整的化学反应。
(1)假设硝酸的还原产物只有一种,利用其中五种物质组成一个完整的化学反应,请写出该化学方程式,并标明电子转移的方向与数目:
__________________________________________________________________________;
(2)上述所写的反应中,被还原的元素是______________,氧化产物是_________________。
(3)如果用六种物质组成一个完整的化学反应,则该反应中还原产物必有__________种,若假定该反应中NH4NO3与N2O的物质的量之比为1∶1,那么该反应中还原剂与氧化剂的物质的量之比为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com