
| A. | HCO3-+H2O?H2CO3+OH- | B. | HS-+H2O?S2-+H3O- | ||
| C. | HCO3-+H2O?H3O++CO32- | D. | H3PO4?3H++PO43+ |
分析 A.碳酸氢根离子水解生成碳酸和氢氧根离子;
B.水合氢离子H3O-书写错误;
C.碳酸氢根离子电离出氢离子和碳酸根离子;
D.多元弱酸应分步电离.
解答 解:A.HCO3-+H2O?H2CO3+OH-碳酸氢根离子水解生成碳酸和氢氧根离子,属于水解反应,电离方程式为:HCO3-?H++CO32-或HCO3-+H2O?H3O++CO32-,故A错误;
B.HS-电离方程式为:HS-+H2O?S2-+H3O+,故B错误;
C.碳酸氢根离子部分电离,电离方程式:HCO3-+H2O?H3O++CO32-或HCO3-?H++CO32-,故C正确;
D.H3PO4?H++H2PO4-,H2PO4-?H++HPO42-,HPO42-?H++PO43-,故D错误;
故选C.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 水的生成与水的电解是可逆反应 | |
| B. | 实验室用H2O2制O2,加入MnO2后,反应速率明显加快 | |
| C. | 反应2SO2+O2═2SO3中,可以通过改变反应条件让SO2、O2完全转化为SO3 | |
| D. | 金属钠与足量水反应,增加水的量能加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 聚乙烯可发生加成反应 | |
| C. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 | |
| D. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| PH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

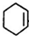 、B
、B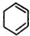 .
.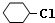 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O,
+NaCl+H2O, +2Cl2→
+2Cl2→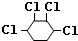 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Q1+3Q2<2Q3 | B. | Q1+Q2<Q3 | C. | 3Q1+Q2<6Q3 | D. | 3Q1+Q2<2Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
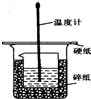 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程 中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com