
| A. | ①=④>③=② | B. | ①=④>③>② | C. | ①>④>③>② | D. | ④>①>③>② |
分析 先根据n=CV计算溶质的物质的量,再根据溶质的电离和水解分析带电微粒的多少.
解答 解:等体积,等物质的量浓度的4种稀溶液,根据n=CV知,各溶质的物质的量相等.
Na2SO4、NaHSO3、Na2S是强电解质,在水中完全电离;Na2SO4、Na2S中阳离子和阴离子个数比为2:1,NaHSO3中阳离子和阴离子个数比为1:1,所以硫酸钠和硫化钠的溶液中阴阳离子数大于亚硫酸氢钠溶液中的阴阳离子数;硫酸钠是强酸强碱盐,在水中不水解,硫化钠是强碱弱酸盐,在水中水解导致溶液中带电荷的微粒数增多,所以硫化钠溶液中的带电微粒数大硫酸钠溶液中的带电微粒数;亚硫酸是弱电解质,只有部分电离,所以亚硫酸溶液中带电微粒数最少,所以①Na2SO4 ②H2SO3 ③NaHSO3 ④Na2S中含带电微粒数由多到少的顺序是④>①>③>②.
故选D.
点评 本题考查了溶液中带电微粒多少的判断,难度较大,注意:强酸弱碱盐或强碱弱酸在水中以电离为主,水解是微弱的.


科目:高中化学 来源: 题型:选择题
| A. | 氨气可以用浓硫酸干燥也可用碱石灰干燥 | |
| B. | 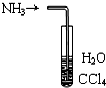 用如图装置吸收NH3可防止倒吸 用如图装置吸收NH3可防止倒吸 | |
| C. | 氨水能导电,所以NH3是电解质 | |
| D. | 氨气可以使湿润的蓝色石蕊试纸变红,依此可检验氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
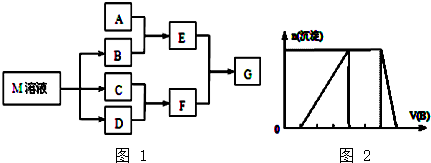
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 | |
| B. | 聚乙炔用I2或Na等做掺杂处理后可形成一种导电塑料,该导电塑料是一种纯净物,有固定的熔点、沸点 | |
| C. | 2014年诺贝尔化学奖授予美国科学家埃里克•贝齐格、威廉•莫纳和德国科学家斯特凡•黑尔,以表彰他们为发展超分辨率荧光显微镜所作的贡献,他们的研究允许了人类观察病毒以至细胞内的蛋白质 | |
| D. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
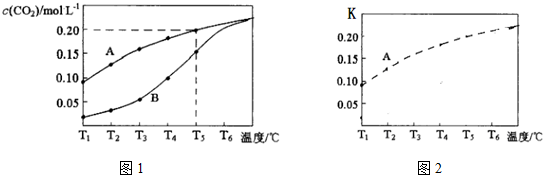
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可使用填埋法处理未经分类的生活垃圾 | |
| B. | 光化学烟雾的形成与汽车尾气中的氮氧化物有关 | |
| C. | 光导纤维都是有机高分子化合物 | |
| D. | “鸟巢”使用钒氮合金钢,该合金熔点、硬度和强度均比纯铁高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{{m}^{2}}{n}$ | B. | $\frac{{m}^{2}}{m+n}$ | C. | $\frac{{m}^{2}}{n-m}$ | D. | $\frac{{n}^{2}}{{m}^{3}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(CH3CO0-) | |
| B. | 加水稀释时$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$增大 | |
| C. | 与pH=12的NaOH溶液等体积混合后,溶液呈酸性 | |
| D. | 加入醋酸钠固体可抑制醋酸的电离,但电离常数Ka不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com