
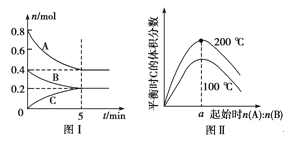
【题目】在容积为2 L的恒容密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图Ⅰ表示200 ℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是 ( )
zC(g),图Ⅰ表示200 ℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A)∶n(B)的变化关系。则下列结论正确的是 ( )
A.图Ⅱ所知反应xA(g)+yB(g)![]() zC(g)的ΔH<0,且a=2
zC(g)的ΔH<0,且a=2
B.200 ℃时,反应从开始到平衡的平均速率v(B)=0.02 mol·L-1·min-1
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He的瞬间,v正>v逆
D.200 ℃时,向容器中充入2 mol A和1 mol B,达到平衡时,A的体积分数等于0.5
【答案】B
【解析】
试题分析:A.由图像可知:升高温度,平衡时C的体积分数增大,说明升高温度化学平衡向正反应方向移动,根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,则正反应方向为吸热反应。所以△H>0,根据图Ⅰ所示可知该反应的方程式为2A+B![]() C,只有当两种反应物按照方程式的计量数的关系加入时生成物C达到平衡时含量才会最高,则a=2,A错误;B.200℃时,反应从开始到平衡的平均速率v(B)={(0.4-0.2) mol÷2 L}÷5 min=0.02 mol/(L·min),B正确;C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,由于平衡混合物中各组分的浓度没变,所以平衡不移动,v(正)=v(逆),C错误;D.由图Ⅰ可知在200℃时,若加入0.8mol A和0.4mol B,达到平衡时A的含量为0.5。若向容器中充入2 mol A 和1 mol B,即增大了反应物的浓度,同时容器内气体的压强增大。根据平衡移动原理:增大压强,化学平衡向正反应方向移动。所以达到平衡时,A 的体积分数小于0.5,D错误;答案选B。
C,只有当两种反应物按照方程式的计量数的关系加入时生成物C达到平衡时含量才会最高,则a=2,A错误;B.200℃时,反应从开始到平衡的平均速率v(B)={(0.4-0.2) mol÷2 L}÷5 min=0.02 mol/(L·min),B正确;C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,由于平衡混合物中各组分的浓度没变,所以平衡不移动,v(正)=v(逆),C错误;D.由图Ⅰ可知在200℃时,若加入0.8mol A和0.4mol B,达到平衡时A的含量为0.5。若向容器中充入2 mol A 和1 mol B,即增大了反应物的浓度,同时容器内气体的压强增大。根据平衡移动原理:增大压强,化学平衡向正反应方向移动。所以达到平衡时,A 的体积分数小于0.5,D错误;答案选B。


科目:高中化学 来源: 题型:
【题目】辣椒素是辣椒的活性成分,可在口腔中产生灼烧感,能够起到降血压和胆固醇的功效,进而在很大程度上预防心脏病,也能缓解肌肉关节疼痛。辣椒素酯类化合物的结构可以表示为:
 (R为烃基)
(R为烃基)
其中一种辣椒素酯类化合物J的合成路线如下:
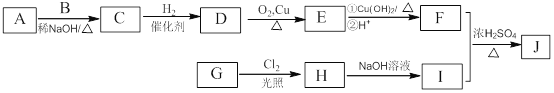
已知:
①A、B和E为同系物,其中B的相对分子质量为44,A和B核磁共振氢谱显示都有两组峰;
②化合物J的分子式为C15H22O4;
③
回答下列问题:
(1)G所含官能团的名称为 。
(2)由A和B生成C的化学方程式为 。
(3)由C生成D的反应类型为 ,D的化学名称为 。
(4)由H生成I的化学方程式为 。
(5)J的结构简式为 。
(6)G的同分异构体中,苯环上的一氯代物只有一种的共有 种(不含立体异构),核磁共振氢谱显示2组峰的是 (写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 甲醛的水溶液具有杀菌、防腐性能
B. 煤进行气化和液化加工可获得清洁燃料
C. 蚕丝和核酸都属于天然高分子化合物
D. 合成纤维和光导纤维都是新型有机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A. NH3可用作制冷剂 B. 过氧化氢有氧化性,不能用于人体消毒
C. S的氧化性比Cl2的氧化性强 D. 电解饱和食盐水制备金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A和B两种有机物可以互溶,有关性质如下
密度(20℃) | 熔点(℃) | 沸点(℃) | 溶解性 | |
A | 0.7893 | -117.3 | 78.5 | 与水以任意比混溶 |
B | 0.7137 | -116.6 | 34.5 | 不溶于水 |
(1)要除去A和B的混合物中的少量B,可采用________方法即可得到A。
A.蒸馏 B.重结晶 C.萃取 D.加水充分振荡,分液
(2)将有机物A置于氧气流中充分燃烧,A和氧气恰好完全反应消耗氧气6.72L(标准状况),生成5.4g H2O和8.8g CO2,则该物质的分子式是______;已知有机物A的核磁共振氢谱如下图所示,则A的结构简式为_______________。以A为原料可以合成M,M可做内燃机的抗冻剂,M与A所含碳原子数相等,M的官能团与A相同,但官能团数目是A的两倍,请写出以A为原料制取M的合成路线:_______________。

(3)若质谱图显示B的相对分子质量为74,红外光谱如图所示,则B的结构简式为____________。

(4)准确称取一定质量的A和B的混合物,在足量氧气中充分燃烧,将产物依次通过足量的无水氯化钙和碱石灰,发现质量分别增重14.4g和26.4g。计算混合物中A和B的物质的量之比___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫和碳及其化合物广泛存在于自然界中,并被人们广泛利用。回答下列问题:
(1)当基态原子的电子吸收能量后,电子会发生____,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为__________。硫所在周期中,第一电离能最大的元素是___________。(填元素符号)
(2)写出一个与CO2具有相同空间结构和键合形式的分子的电子式__________________。
(3)H2S中S原子的杂化类型是__________;H2S的VSEPR模型名称为_________;H2S的键角约为94°,H2O的键角为105°,其原因是___________________________。
(4)科学家通过X射线推测胆矾结构示意图1如下:


其中含有________个配位键,___________个氢键。
(5)已知Zn和Hg同属IIB族元素,火山喷出的岩浆是一种复杂的混合物,冷却时,许多矿物相继析出,其中所含的ZnS矿物先于HgS矿物析出,原因是_________________________________。
(6)碳的另一种同素异形体—石墨,其晶体结构如上图2所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为____个,已知石墨的密度为pg·cm-1,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为____cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组设计如下实验装置探究电化学原理,装置Ⅰ中Zn电极产生ZnO,下列说法正确的是

A. Cu电极质量增加
B. 装置Ⅱ将化学能转变为电能
C. 装置Ⅰ中OH-向多孔电极移动
D. 多孔电极的电极反应式为:O2+4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学通过以下步骤提取海带中的碘:
①将海带晒干灼烧成灰 ②将海带浸泡得其悬浊液
③过滤得含碘离子的溶液 ④向该溶液中加入适量Cl2置换出碘
⑤对含碘溶液进行一系列的提取后得碘单质
(1)灼烧过程在下列哪种仪器中(_____)
A. 烧杯 B. 试管 C. 蒸发皿 D. 坩埚
(2)过滤用到的三种玻璃仪器主要是____________________。
(3)用有机溶剂将碘从水中提取出来需要用到下列哪套装置____。

若用四氯化碳作溶剂进行提取,则分层后下层物质为___________。
(4)写出步骤④中发生反应的离子方程式:_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com