
A、 |
B、 |
C、 |
D、 |
科目:高中化学 来源: 题型:
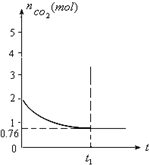 一定温度下2升的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应:
一定温度下2升的恒容容器甲中,加入2moL碳和2moLCO2发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| Cu/O2/△ |
| 新制Cu/(OH)2/煮沸 |
 的方法与过程:
的方法与过程:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、质子数相同的原子,其核外电子排布也相同 |
| B、质量数相同的原子,其化学性质一定相同 |
| C、金属性越活泼,其原子在反应中越易失去电子 |
| D、非金属性越活泼,其阴离子越难失去电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中溶质微粒作有规律的运动,胶体粒子运动无规律 |
| B、溶液中溶质微粒一定不带电,胶体中分散质微粒带电荷 |
| C、溶液中通过一束光,无特殊现象,而胶体中有“光亮的通路” |
| D、溶液呈电中性,胶体带有电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丙烯的结构简式:C3H6 |
B、氢氧根离子的电子式: |
C、氯原子的结构示意图: |
| D、红磷在过量Cl2中燃烧生成PCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性氧化物在一定条件下,都可以与碱反应生成盐和水 |
| B、一种元素可能有多种氧化物,但是同种化合价只对应一种氧化物 |
| C、酸根离子中不可能含有金属元素 |
| D、还原产物只有还原性,氧化产物只有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯不能使酸性高锰酸钾溶液褪色 |
| B、苯跟浓硝酸、浓硫酸混合加热,可制得硝基苯 |
C、苯生成 为加成反应 为加成反应 |
| D、苯在催化剂作用下能跟氢气发生加成反应,生成环己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com