
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
分析 常温下,某溶液中由水电离的[H+]和[OH-]的乘积为1.0×10-22 mol2•L-2,则水电离的[H+]=[OH-]=1.0×10-11mol/L,该溶液为酸性或碱性溶液,溶液中存在电离氢离子或氢氧根离子,
A.四种离子之间不反应,都不与氢离子反应;
B.四种离子之间不反应,都不与氢氧根离子反应;
C.四种离子之间不反应,都不与氢离子反应;
D.铵根离子与硅酸根离子发生双水解反应,铵根离子与氢氧根离子、硅酸根离子与氢离子反应.
解答 解:常温下,某溶液中由水电离的[H+]和[OH-]的乘积为1.0×10-22 mol2•L-2,则水电离的[H+]=[OH-]=1.0×10-11mol/L,该溶液为酸性或碱性溶液,溶液中存在电离氢离子或氢氧根离子,
A.Al3+、Na+、NO3-、Cl-之间不反应,都不与氢离子反应,在酸性溶液中能够共存,故A错误;
B.K+、Na+、Cl-、CO32-之间不反应,都不与氢氧根离子反应,在碱性溶液中能够共存,故B错误;
C.NH4+、Na+、Cl-、SO42-之间不反应,都不与氢离子反应,在酸性溶液中能够共存,故C错误;
D.NH4+与氢氧根离子反应,SiO32-与氢离子反应,NH4+、SiO32-之间发生双水解反应,在溶液中一定不能大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | pH=2的溶液中:NH4+、Na+、Cl-、Cu2+ | |
| B. | 加入KSCN显红色的溶液:K+、NH4+、Cl-、CO32- | |
| C. | 无色溶液中:K+、CH3COO-、HCO3-、MnO4- | |
| D. | 含有大量NaClO的水溶液中:Fe2+、Cl-、Ca2+、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
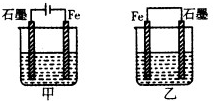 如图所示装置,均盛有等体积等浓度的稀硫酸,工作一段时间后当甲乙装置中通过电子的物质的量相同时,下列说法正确的是( )
如图所示装置,均盛有等体积等浓度的稀硫酸,工作一段时间后当甲乙装置中通过电子的物质的量相同时,下列说法正确的是( )| A. | A、甲乙两装置中的石墨电极分别是阴极、负极 | |
| B. | 铁棒的腐蚀程度:甲>乙 | |
| C. | 石墨电极上发生反应的电极反应式相同 | |
| D. | 溶液的pH:甲减小,乙增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4?Ba2++SO42- | B. | HF═H++F- | ||
| C. | HI?H++I- | D. | NaHCO3═Na++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO3->BrO3->Cl2>Fe3+>I2 | B. | BrO3->Cl 2>ClO3->I2>Fe3+ | ||
| C. | BrO3->ClO3->Cl2>Fe3+>I2 | D. | BrO3->ClO3->Fe3+>Cl2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
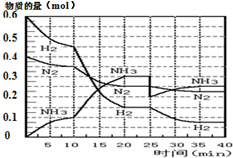 氨的合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.4KJ•mol-1.现在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图.
氨的合成原理为:N2(g)+3H2(g)?2NH3(g);△H=-92.4KJ•mol-1.现在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图.| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v1、v2、K1、K2同时增大 | B. | v1、v2、K1、K2同时减小 | ||
| C. | v1、v2增大,K1增大,K2减小 | D. | v2减小,v1增大,K1增大,K2减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com