
| A. | ①中水银“积变又还成丹砂”说明水银发生了还原反应 | |
| B. | ②中反应的离子方程式为:2Fe+3Cu2+=2Fe3++3Cu | |
| C. | 根据①可知温度计打破后可以用硫粉覆盖水银,防止中毒 | |
| D. | 水银能跟曾青发生置换反应生成单质铜 |
分析 ①“丹砂(HgS)烧之成水银”,反应为HgS$\frac{\underline{\;加热\;}}{\;}$Hg+S;“积变又还成丹砂”发生的反应为:Hg+S=HgS;②“以曾青涂铁,铁赤色如铜”发生的反应为:CuSO4+Fe=FeSO4+Cu,据此分析.
解答 解:①“丹砂(HgS)烧之成水银”,反应为HgS$\frac{\underline{\;加热\;}}{\;}$Hg+S;“积变又还成丹砂”发生的反应为:Hg+S=HgS;②“以曾青涂铁,铁赤色如铜”发生的反应为:CuSO4+Fe=FeSO4+Cu.
A、①中水银“积变又还成丹砂”是水银发生了氧化反应,由Hg生成HgS,故A错误;
B、②中发生的反应为:CuSO4+Fe=FeSO4+Cu,离子方程式为:Cu2++Fe=Fe2++Cu,故B错误;
C、根据①可知温度计打破后可以用硫粉覆盖水银,则会发生反应:Hg+S=HgS,生成的HgS无毒,故能防止中毒,故C正确;
D、曾青为硫酸铜,水银能和硫酸铜发生置换反应生成铜,故D错误.
故选C.
点评 本题主要考查的是元素化合物的性质,题目的情景设计较新颖,予化学知识于古文字中,注意古文的理解和化学物质性质的分析判断,题目难度中等.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 取等体积、pH相同的醋酸和盐酸分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m<n | |
| B. | 将pH=2的CH3COOH溶液加水稀释,水的电离平衡也向右移动 | |
| C. | 常温下,将pH=2的H2SO4与pH=12的NH3•H2O溶液等体积混合后,混合液pH<7 | |
| D. | 某温度下水的离子积为1×10-12,若使pH=1的H2SO4与pH=12的NaOH溶液混合后溶液呈中性,则两者的体积比为1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
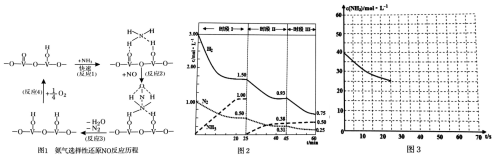
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 190 | B. | 218 | C. | 436 | D. | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Na+、Cu2+、NO3-、Cl- | |
| B. | 在pH=4的溶液中:Na+、K+、OH-、Cl- | |
| C. | 在含Ba2+的溶液中:H+、Na+、Cl-、SO42- | |
| D. | 与Fe反应产生气体的溶液:Na+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
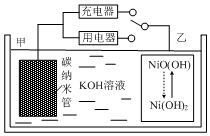 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A. | 放电时,甲电极为正极,OH-移向乙电极 | |
| B. | 放电时,乙电极反应为:Ni(OH)2+OH--e-=NiO(OH)+H2O | |
| C. | 充电时,电池的碳电极与直流电源的正极相连 | |
| D. | 电池总反应为H2+2NiOOH$?_{充电}^{放电}$2Ni(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
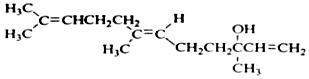 关于橙花醇叙述错误的是( )
关于橙花醇叙述错误的是( )| A. | 可使酸性 KMnO4溶液褪色 | |
| B. | 橙花醇中含有2种官能团 | |
| C. | 在浓硫酸催化下加热脱水,生成的产物不止一种 | |
| D. | 1mol橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗240g溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
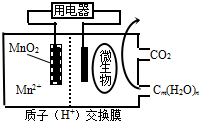
| A. | 放电过程中,H+从正极区移向负极区 | |
| B. | 分子组成为Cm(H2O)n的物质一定是糖类 | |
| C. | 微生物所在电极区放电时发生还原反应 | |
| D. | 左边电极反应式为:MnO2+4H++2e-=Mn2++2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com