
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | 向氯化铁溶液中加入NaOH溶液,可制得Fe(OH)3胶体 | |
| C. | 固体的NaCl不导电,熔融态的NaCl可以导电 | |
| D. | 在河流入海口处易形成三角洲原理与胶体的性质无关 |
分析 A.NaClO在水中能完全电离是强电解质;
B.实验室制备氢氧化铁胶体是把饱和氯化铁溶液滴入沸水中加热到呈红褐色液体;
C.固态的NaCl不存在自由移动的离子;
D.江河入海口三角洲的形成是胶体聚沉的结果.
解答 解:A.NaClO属于盐,在水中能完全电离是强电解质,故A错误;
B.实验室制备氢氧化铁胶体是把饱和氯化铁溶液滴入沸水中加热到呈红褐色液体,氯化铁与氢氧化钠反应生成氢氧化铁沉淀,故B错误;
C.固态的NaCl不存在自由移动的离子,所以不导电;NaCl在熔融状态电离产生自由移动的离子,所以能够导电,故C正确;
D.江河中的泥浆属于胶体,江河入海口三角洲的形成是胶体聚沉的结果,故D错误.
故选C.
点评 本题考查胶体的性质、电解质的判断,明确电解质的概念是解题关键,注意物质导电的条件,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①③⑤⑦⑧ | B. | ②④⑦ | C. | ①⑥ | D. | ②④⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
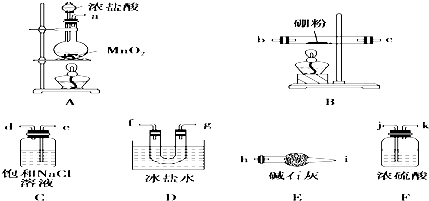
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 摩尔质量为313.5 g | B. | 属于芳香烃 | ||
| C. | 分子式为C12H19Cl3N2O | D. | 不能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  曲线可表示向0.1 mol/L CH3COONa溶液中加水稀释的过程中OH-浓度随溶液体积的变化趋势 | |
| B. | 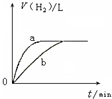 曲线a、b分别表示过量纯锌、过量粗锌(含Cu、C杂质)跟同浓度等体积盐酸反应过程中产生H2体积的变化趋势 | |
| C. |  曲线c、d分别表示等质量的铝分别跟过量烧碱溶液、过量盐酸反应过程中产生H2体积的变化趋势 | |
| D. | 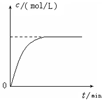 曲线可表示足量锌与一定量稀醋酸反应过程中,Zn2+浓度的变化趋势(假设反应过程中溶液体积保持不变) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S?2H++S2- | B. | KHSO4═K++HSO4- | ||
| C. | CH3COOH?H++CH3COO- | D. | NaH2PO4?Na++H2PO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸汽和硫固体分别在氧气中完全燃烧,后者放出的热量少 | |
| B. | 1molH2在足量氯气中完全燃烧所放出的热量,是H2的燃烧热 | |
| C. | HCl与NaOH反应的中和热△=-57.3kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-2×(-57.3)kJ•mol-1 | |
| D. | 一定条件下,0.2molSO2(g)与0.1molO2(g)混合充分反应时放出的热量为18kJ,则有SO2(g)+O2(g)═2SO3(g)△H=-180kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+0.6mol/L | B. | CO32- 0.2 mol/L | C. | Mg2+0.4 mol/L | D. | Ba2+0.4mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com