
下列说法中正确的是( )
A.s区、d区、ds区都是金属元素 B.p区都是主族元素
C.所有族中IIIB中元素种类最多 D.最外层电子数为2的元素都分布在s区
科目:高中化学 来源:2015-2016学年湖南省高一下期中化学试卷(解析版) 题型:填空题
如表所示是元素周期表示意图的一部分,根据表中10种元素,用元素符号或化学式填空。
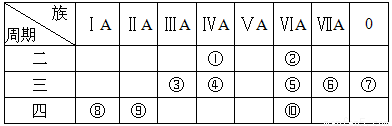
(1)①~⑩元素中,金属性最强的是 (填元素符号);化学性质最不活泼的是 (填元素符号)。
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是 (填元素符号),该水化物与NaOH溶液反应的离子方程式为 。
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的是 (填化学式),碱性最强的是 (填化学式)。
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是 。(填离子符号)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北武汉华中师大一附高一下期中化学试卷(解析版) 题型:选择题
砹是原子半径最大的卤族元素,下列预测一定不正确的是
A.NaAt易溶于苯和四氯化碳等有机溶剂 B.At的最高化合价为+7价
C.At2是一种有色固体,与H2反应十分缓慢 D.AgAt是有色固体,见光易分解
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:选择题
检验溴乙烷中含有溴元素存在的实验步骤、操作和顺序正确的是( )
①加入AgNO3溶液 ②加入NaOH溶液加热 ③加入适量HNO3 ④冷却
A. ①②④③ B.②④③① C.②④① D.②③④①
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北沙市高二下第四次半月考化学试卷(解析版) 题型:选择题
下图为冰晶体的结构模型,大球代表O原子,小球代表H原子,下列有关说法正确的是( )
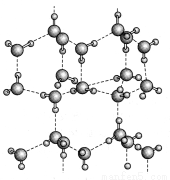
A.冰晶体中每个水分子与另外2个水分子形成四面体
B.冰晶体具有空间网状结构,是原子晶体
C.水分子间通过H—O···H键形成冰晶体
D.冰晶体熔化时,水分子之间的空隙增大
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三5月月考理综化学试卷(解析版) 题型:填空题
雾霾天气肆虐给人类健康带来了严重影响。燃煤和汽车尾气 是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g) 2C02(g)+N2 (g) △H <0 。
2C02(g)+N2 (g) △H <0 。
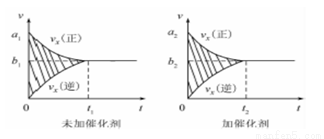
①该反应的速率时间图像如右图中左图所示。若其他条件不变,仅在反应前加入合适的催化剂,则其速率时间图像如右图中右图所示。以下说法正确的是 (填对应字母)。
A.a1>a2 B.b1 <b2 C.t1>t2
D.右图中阴影部分面积更大 E.左图中阴影部分面积更大
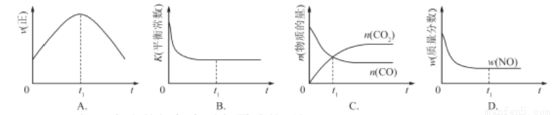
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。已知:CH4(g)+2N02(g) = N2(g)+C02(g)+2H20(g) △H=-867 kJ/mol
2N02(g)= N204(g) △H= - 56.9 kJ/mol H20(g) = H20(l) △H = - 44.0 kJ/mol
写出CH4催化还原N204 (g)生成N2和H20(1)的热化学方程式: 。
(3)CH4和H20(g)在催化剂表面发生反应CH4 + H20 = C0 + 3H2 ,该反应在不同温度下的化学平衡常数如下表:
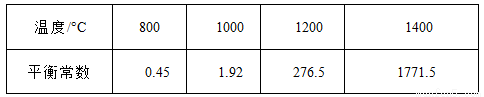
①该反应是 反应(填“吸热”或“放热 ”)。
②T℃时,向1L密闭容器中投入1mol CH4 和1mol H20(g),平衡时C(CH4)=0.5 mol·L-1 , 该温度下反应CH4 + H20 = CO+3H2的平衡常数K= 。
(4)甲烷燃料电池可以提升能量利用率。如图是利用甲烷燃料电池电解100mL lmol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24 L(设电解后溶液体积不变)。
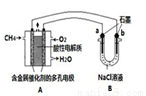
①甲烷燃料电池的负极反应式: 。
②电解后溶液的pH = , (忽略氯气与氢氧化钠溶液反应)。
③阳极产生气体的体积在标准状况下是 L。
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三5月月考理综化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值,下列叙述正确的是
A.室温下向1LpH=1的醋酸溶液中加水,所得溶液的H+数目大于0.1NA
B.60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA
C.某无水乙醇与足量金属钠反应生成5.6LH2,该乙醇分子中共价键总数为4NA
D.已知C2H4(g)+H2(g)=C2H6(g)△H=-137.0kI/mol,乙烯与H2加成时放出68.5kJ热量,则反应过程中被破坏的碳原子之间共用电子对数目为NA
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三考训练四理综化学试卷(解析版) 题型:实验题
钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质)。

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表:
| Fe3+ | Co2+ | Co3+ | Al3+ |
pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式 。
(2)步骤Ⅱ中Co2O3与盐酸反应的离子方程式 。
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应调节溶液的pH范围是 ;废渣中的主要成分为 。
(4)步骤Ⅲ中NaF参与的反应对步骤Ⅳ所起的作用是
(5)在空气中加热5.49 g草酸钴晶体(CoC2O4·2H2O)样品,[ M (CoC2O4·2H2O) = 183 g/mol ] 受热过程中不同温度范围内分别得到一种固体物质,其质量如下表。
温度范围/℃ | 固体质量/ g |
150~210 | 4.41 |
290~320 | 2.41 |
890~920 | 2.25 |
经测定,210~290℃过程中产生的气体只有CO2,此过程发生反应的化学方程式是
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二下期中理综化学试卷(解析版) 题型:实验题
实验室用下列仪器组装一套蒸馏石油的装置,并进行蒸馏得到汽油和煤油。
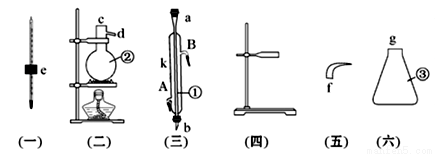
(1)写出下列仪器的名称:
①__________________;②___________________;③_________________。
(2)将以上仪器按从左到右顺序,用字母a、b、c……进行连接:
e接__________;_________接_________;_________接_________
(3)①仪器的A口是__________,B口是__________。
(4)蒸馏时,温度计水银球应在______________________(位置)。
(5)在②中注入原油后,加几片碎瓷片的目的是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com