
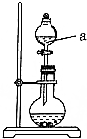
 某化学小组同学发现84消毒液(主要成分为NaClO)与洁厕剂(主要成分为盐酸)室温下混合有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2.
某化学小组同学发现84消毒液(主要成分为NaClO)与洁厕剂(主要成分为盐酸)室温下混合有Cl2生成,于是尝试在实验室利用该反应原理制取Cl2.分析 浓盐酸易挥发,生成的氯气中混有HCl,NaHCO3溶液pH=8,说明水解呈碱性,又室温下H2CO3的电离常数K1=4.2×10-7,K2=5.6×10-11,结合K2计算.
解答 解:有装置可知a为分液漏斗,浓盐酸易挥发,生成的氯气中混有HCl,氯气通入水之前应先除杂,以防止干扰实验结论,
室温下H2CO3的电离常数K1=4.2×10-7,K2=5.6×10-11,
$\frac{c({H}^{+})c(C{{O}_{3}}^{2-})}{c(HC{{O}_{3}}^{-})}$=K2=5.6×10-11,所以c(CO32-):c(HCO3-)=$\frac{5.6×1{0}^{-11}}{1{0}^{-8}}$=5.6×10-3,
故答案为:分液漏斗;氯气中混有HCl;5.6×10-3:1.
点评 本题考查氯气的制备以及弱电解质的电离,为高频考点,侧重于学生分析、实验和计算能力的考查,注意把握实验的严密性以及弱电解质的电离特点,难度中等.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:选择题
| A. | 能导电的有①②⑤⑥ | |
| B. | 属于电解质的有⑤⑦⑧ | |
| C. | 属于强电解质的有⑤⑥⑧ | |
| D. | 既不属于电解质又不属于非电解质的有①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| A | 常温下单质能与水剧烈反应,所得溶液呈强碱性 |
| B | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| C | 第三周期元素的原子中半径最小 |
| D | D的一种同位素可测定文物年代 |
| E | 次外层电子数比最外层电子数多2个 |
 ,该氢化物溶于水,水溶液呈碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.
,该氢化物溶于水,水溶液呈碱性的原因(用电离方程式表示)NH3•H2O?NH4++OH-.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B的转化率为20% | |
| B. | 平衡时A的浓度为1.50 mol•L-1 | |
| C. | x=1 | |
| D. | 达到平衡时,在相同温度下容器内混合气体的压强是反应前的85% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com