
下列各组中两个溶液间的反应,均可用同一离子方程式表示的是 ( )
A.CH3COOH和Na2CO3与CH3COOH和NaHCO3
B.AgNO3和HCl与Ag2SO3和HCl
C.BaCl2和Na2SO4 与Ba(OH)2与H2SO4
D.KOH和CH3COOH与Ba(OH)2与CH3COOH
科目:高中化学 来源:2016届安徽省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列溶液中相应关系正确的是( )
A.0.2 mol·L-1CH3COONa溶液和0.1 mol·L-1HCl溶液等体积混合后:
c(CH3COO-)>c(Na+)>c(Cl-)>c(H+)>c(OH-)
B.pH=3的盐酸和NaNO3的混合溶液中:c(Na+)=c(Cl -)
C.0.1 mol·L-1NaHCO3 溶液中: c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
D.含SO42-、NH4+、H+、OH-的溶液中可能存在:c(H+)>c(SO42-)>c(NH4+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏银川唐徕回民中学高一上10月化学卷(解析版) 题型:选择题
下列叙述正确的是
A.1mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1mol任何物质体积均为22.4L
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第三次月考化学试卷(解析版) 题型:选择题
A、B、C、D、E五种短周期元素,其原子序数逐渐增大。元素A的单质是密度最小的气体,元素B的单质存在两种以上同素异形体,且其中一种是自然界中硬度最大的单质,元素D的最外层电子数是次外层电子数的三倍。B、C、D、E四种元素均能与A形成电子数相等的四种分子,且化合物中各原子的个数比如下表:
化合物 | 甲 | 乙 | 丙 | 丁 |
原子个数比 | B∶A=1∶3 | C∶A=1∶2 | D∶A=1∶1 | E∶A=1∶1 |
下列说法正确的是( )
A.元素E在元素周期表中的位置为第二周期第ⅦA族
B.原子半径:A<B<C<D
C.A、C、E中三种元素或任意两种元素形成的物质中只可能含有共价键
D.A、B、C、D四元素中的三种能形成多种与甲分子电子数相等的化合物
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:简答题
短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(一)(1)D在周期表中的位置是 ,写出实验室制备单质F的离子方程式 。
(2)化学组成为BDF2的电子式为: ,A、C、F三种元素形成的化合物CA4F为 化合物(填 “离子”或“共价”)。
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为: 。
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是 (用元素离子符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性 于F(填“强”或“弱”),并用化学方程式证明上述结论 。
(二)以CA3代替氢气研发氨燃料电池是当前科研的一个热点。
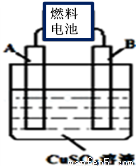
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 CA3+3O2=2C2+6H2O.该电池负极的电极反应式为 ;每消耗3.4g CA3转移的电子数目为 。
(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
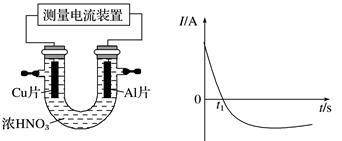
图1 图2
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是 ,溶液中的H+向 极移动(填“正”或“负”),t1时,原电池中电子流动方向发生改变,其原因是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高一上期中化学试卷(解析版) 题型:选择题
某同学用托盘天平称量锌粒24.4g(1g以下用游码),他把锌粒放在右盘,砝码放在左盘,当天平平衡时,所称取的锌粒的实际质量应是( )
A.24.4g B.25.5g C.23.6g D.24g
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③沸点:H2Se>H2S>H2O
④结合H+能力:OH->CH3COO->I-
A.①③ B.②③ C.①④ D.②④
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上第三次模拟化学试卷(解析版) 题型:选择题
下列制备和收集气体的实验装置合理的是( )
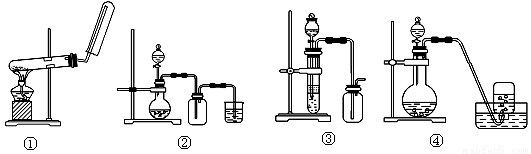
A.装置①:用氯化铵和氢氧化钙制NH3
B.装置②:用铜和稀硝酸制NO
C.装置③:用锌粒和稀硫酸制H2
D.装置④:用双氧水和二氧化锰制O2
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三上学期12月月考理综化学试卷(解析版) 题型:填空题
二甲醚(CH3OCH3)是一种重要的清洁燃料气,其储运、燃烧安全性、理论燃烧温度等性能指标均优于液化石油气,也可用作燃烧电池,具有很好的发展前景。
(1)已知H2、CO和CH3OCH3的燃烧热(ΔH)分别为-285.5kJ/mol、-283kJ/mol和-1460.0 kJ/mol,则工业上利用水煤气成分按1:1合成二甲醚的热化学方程式为:____________。
(2)工业上采用电浮远凝聚法处理污水时,保持污水的pH在5.0,通过电解生成Fe(OH)3胶体,吸附不溶性杂质,同时利用阴极产生的H2,将悬浮物带到水面,利于除去。实验室以二甲醚燃料电池模拟该方法设计的装置如下图所示:
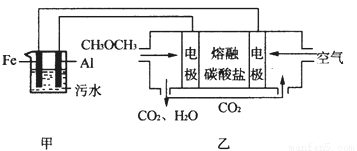
①乙装置以熔融碳酸盐为电解质,稀土金属材料为电极。写出该燃料电池的正极电极反应式 __________________;下列物质可用做电池熔融碳酸盐的是 ______。
A.MgCO3 B.Na2CO3 C.NaHCO3 D.(NH4)2CO3
②写出甲装置中阳极产物离子生成Fe(OH)3沉淀的离子方程式____________________ 。
③已知常温下Ksp[Fe(OH)3]=4.0×10-38,电解一段时间后,甲装置中c(Fe3+)= ___________。
④已知:H2S的电离平衡常数:K1=9.1×10-8、K2=1.1×10-12;H2CO3的电离平衡常数:K1=4.31×10-7、K2=5.61×10-11。测得电极上转移电子为0.24mol时,将乙装置中生成的CO2通入200mL 0.2mol/L的Na2S溶液中,下列选项正确的是______
A.发生反应的离子方程式为:CO2+S2-+H2O=CO32-+H2S
B.发生反应的离子方程式为:CO2+S2-+H2O=HCO3-+HS-
C.c(Na+)=2[c(H2S)+c(HS-)+c(S2-)
D.c(Na+)+c(H+)=2c(CO32-)+2c(S2-)+c(OH-)
E.c(Na+)>c(HCO3-)>c(HS-)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com