
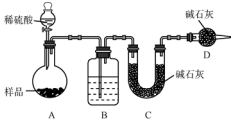
I.下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。

请回答下列问题:
(1)能用作干燥氨气的装置有___________(填字母);
(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有___________(填字母);
(3)在氯气和铁反应实验中,能添加在制氯气和反应装置之间以除去氯气中氯化氢等杂质气体的装置有___________(填字母);
(4)若用C装置作二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶的作用是__________。
II.我国化学家侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:
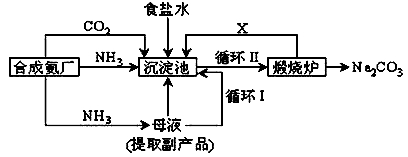
(1) 沉淀池中发生的化学反应方程式是______________________。
(2) 写出上述流程中X物质的分子式___________。
(3)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加___________。
(4) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有______________。
a.增大NH4+的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某校课外小组为测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数,甲、乙两组同学分别进行了下列相关实验.
某校课外小组为测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数,甲、乙两组同学分别进行了下列相关实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3和HCl | B. | NaCl和Na2CO3 | C. | H2SO4和BaCl2 | D. | NaCl和Na2SO4 |
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上10月月考化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.40g碳化硅晶体中含有的C—Si的数目为2NA
B.1L 1 mol·L-1 AlCl3溶液中含有的Al3+数目为NA
C.0.1mol熔融的NaHSO4中含有的阳离子为0.2 NA个
D.在标况下,11.2L HCHO中含有π键的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:实验题
I.高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制480mL 0.1000 mol·L-1的酸性KMnO4溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、 。
②下列操作对实验结果的影响偏大的是 (填序号)。
a.加水定容时俯视刻度线
b.容量瓶底部有少量蒸馏水
c.颠倒摇匀后发现凹液面低于刻度线又加水补上
d.天平的砝码生锈
(2)某化学兴趣小组,用新配制的酸性KMnO4溶液来测定某试剂厂生产的FeSO4溶液中Fe2+的物质的量浓度。
①酸性高锰酸钾溶液与FeSO4溶液反应的离子方程式为
②该小组在测定过程中发现,测得的Fe2+的物质的量浓度比标签上的标注值要低,在滴定操作准确的前提下,可能导致该测定结果的原因如下:
猜想一:FeSO4溶液变质;证明方法是
猜想二:
Ⅱ.某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1 mol X在该反应中失去3.01×1023个电子。
(1)写出该反应的化学方程式:________________________;
(2)该反应体系中,若用浓盐酸代替硫酸,用离子方程式表示后果: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学试卷(解析版) 题型:填空题
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g5.00%的NaOH溶液、足量的CuSO4溶液和100g10.00%的K2SO4溶液,电极均为石墨电极。
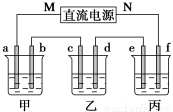
(1)接通电源,经过一段时间后,测得丙中K2SO4质量分数为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为_______________极;
②电极b上发生的电极反应为_______________;
③电极b上生成的气体在标准状况下的体积为_______________L;
④电极c的质量变化是__________g;
⑤电解前后各溶液的pH是否发生变化:
甲溶液______________;乙溶液_____________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一上10月月考化学试卷(解析版) 题型:实验题
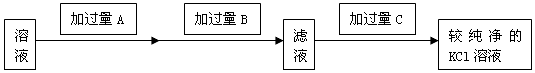
某校探究学习小组同学用含有少量杂质(主要为少量泥沙、CaCl2、MgCl2、Na2SO4等)的粗盐制取“化学纯”级的NaCl,实验前他们设计了如下方案(框图).
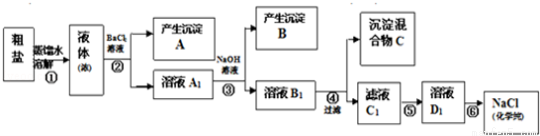
(1)请写出操作第④、⑤步所加试剂名称及第⑥步操作名称:
④_________,⑤_________,⑥_________;
(2)写出第⑤步操作中可能发生反应的化学方程式:________________________;
(3)如何用最简单方法检验第⑤步实验是否达到了目的:________________________;
(4)你认为该设计里哪些步骤调换后不影响实验结果:____________________________;
(5)有同学认为上述实验设计步骤可以简化,请你提出简化的一种设想:_______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com