
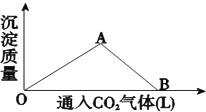
【题目】如图为一定量饱和 Ca(OH)2溶液中通入二氧化碳气体后,产生 CaCO3 白色沉淀的质量与二氧化碳体积之间的关系曲线.
试回答:
OA 段所表示的反应离子方程式是:________,AB 段所表示的反应化学方程式是:________,将 B 处生成的溶液煮沸,可见到的现象是________.
【答案】 Ca2++2OH﹣+CO2=CaCO3↓+H2O CaCO3+CO2+H2O=Ca(HCO3)2 白色沉淀和气体生成
【解析】
在Ca(OH)2溶液中通入二氧化碳气体,先生成CaCO3(不溶于水),再转化为Ca(HCO3)2(能溶于水),加热时Ca(HCO3)2分解又生成了不溶性的CaCO3;据此分析完成各题。
OA段:在Ca(OH)2溶液中通入二氧化碳气体,生成CaCO3(不溶于水),反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O,离子方程式为:Ca2++2OH-+CO2=CaCO3↓+H2O;AB段:当碱消耗完,再通入二氧化碳,二氧化碳与碳酸钙、水继续反应生成Ca(HCO3)2(溶于水),反应化学方程式为:CaCO3+CO2+H2O=Ca(HCO3)2;B处的是Ca(HCO3)2溶液,Ca(HCO3)2不稳定,受热易分解:Ca(HCO3)2=CaCO3↓+CO2↑+H2O,故将B处的溶液煮沸,现象是有白色沉淀和气体生成,故答案为:Ca2++2OH-+CO2=CaCO3↓+H2O;CaCO3+CO2+H2O=Ca(HCO3)2;白色沉淀和气体生成。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】在汽车尾气净化装置里,气体在催化剂表面吸附与释放的过程如图所示.下列说法正确的是( )
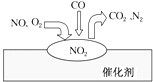
A. NO是该过程的中间产物 B. NO和O2必须在催化剂表面才能反应
C. 汽车尾气的主要污染成分包括CO2和N2 D. 汽车尾气的主要污染物是CO和NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C 为中学常见单质,其中一种为金属;通常情况下,A 为固体,B 为液体,C 为气体。D、 E、F、G、H、X 均为化合物,其中 X 是一种无氧强酸、E 为黑色固体,H 在常温下为液体。它们之间的 转化关系如图所示(其中某些反应条件和部分反应物已略去)。

(1)写出化学式:A____________、D__________、E__________、X________。
(2) 在反应①~⑦中,不属于氧化还原反应的是__________(填编号)。
(3) 反应⑥的离子方程式为__________。
(4)反应⑦的化学方程式为__________,该反应中每消耗 0.3molA,可转移电子__________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以环戊烷为原料制备环戊二烯的合成路线如图,则( )
![]()
A. A的结构简式是![]()
B. ①②的反应类型分别是取代、消去
C. 反应②③的条件分别是浓硫酸加热、光照
D. 酸性KMnO4溶液褪色可证明![]() 已完全转化成
已完全转化成![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所给的方程式写出离子方程式.
(1)Na2CO3+BaCl2═2NaCl+BaCO3↓________
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑________
(3)CO2+2NaOH═Na2CO3+2H2O________
(4)Fe2O3+6HCl═2FeCl3+3H2O________
(5)Zn+2HCl═ZnCl2+H2↑________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气在25℃、101kPa时,在1L水中可溶解0.09mol,实验测得溶于水的Cl2约有![]() 与水反应。请回答下列问题:
与水反应。请回答下列问题:
(1)该反应的离子方程式为________。
(2)算该反应的平衡常数为________(利用离子方程式计算)。
(3)在上述平衡体系中加入少量KOH固体,平衡将________(填“向正反应方向”、“向逆反应方向”或“不”)移动。
(4)如果增大氯气的压强,氯气在水中的溶解度将________(填“增大”、“减小”或“不变”),平衡将________(填“向正反应方向”、“向逆反应方向”或“不”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应的化学方程式中,属于水解反应的是( )
A. H2O+H2O ![]() H3O++OH- B. HCO3-+OH-
H3O++OH- B. HCO3-+OH-![]() H2O+CO32-
H2O+CO32-
C. CO2+H2O ![]() H2CO3 D. CO32-+H2O
H2CO3 D. CO32-+H2O ![]() HCO3-+OH-
HCO3-+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在初始温度为500℃、容积恒定为10L的三个密闭容器中,如图充料发生反应:CO2 (g) +3H2 (g) ![]() CH30H(g)十H2 O (g)△H= -25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是
CH30H(g)十H2 O (g)△H= -25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是

A. 刚开始反应时速率:甲>乙
B. 平衡后反应放热;甲>乙
C. 500℃下该反应平衡常数:K =3×102
D. 若a≠0,则0.9<b<l
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com