
| A. | 1,2-二甲苯也称邻二甲苯 | |
| B. | 氨基乙酸与a-氨基丙酸的混合物一定条件下脱水能生成4种二肽 | |
| C. | 苯与溴水不能发生加成反应,所以两者混合后无明显现象 | |
| D. | C5H10O2属于羧酸的同分异构体有4种 |
分析 A.苯的同系物,含有两个甲基,位置相邻,可以命名为:邻二甲苯,根据有机物的系统命名法,正确名称是:1,2-二甲苯;
B.氨基酸中氨基和羧基去掉一分子水形成肽键;
C.苯能萃取溴水中溴;
D.C5H10O2属于羧酸的同分异构体为丁烷中的1个H原子被-COOH夺取,即由丁基与-COOH构成,其同分异构体数目与丁基异构数目相等;
解答 解:A.1,2-二甲苯中两个甲基,位置相邻,可以命名为:邻二甲苯,故A正确;
B.氨基乙酸和a-氨基丙酸生成二肽,可以生成甘甘二肽、甘丙二肽、丙丙二肽、丙甘二肽,共4种二肽,故B正确;
C.苯能萃取溴水中溴,从而使溴水褪色,故C错误;
D.C5H10O2属于羧酸的同分异构体为丁烷中的1个H原子被-COOH夺取,即由丁基与-COOH构成,其同分异构体数目与丁基异构数目相等,-C4H9异构体有:-CH2CH2CH2CH3,-CH(CH3)CH2CH3,-CH2CH(CH3)CH3,-C(CH3)3,故符合条件的有机物的异构体数目为4.即分子式为C5H10O2属于羧酸的同分异构体数目也有4种,故D正确;
故选C.
点评 本题考查苯的同系物的命名法,同分异构体的书写与判断等,难度中等,关键是形成酯的羧酸与醇的同分异构体的判断.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入乙醇的目的是降低溶剂的极性,促使[Cu(NH3)4]SO4晶体析出 | |
| B. | 该配合物晶体中,N是配位原子,NH3为三角锥形,配位数是4 | |
| C. | 配离子内N原子排列成为平面正方形,可见Cu2+是sp3杂化 | |
| D. | 向该晶体的水溶液中加入浓BaCl2溶液无白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KOH和Al2(SO4)3 | B. | NaOH和Ca(HCO3)2 | C. | NaAlO2和 HCl | D. | K2CO3和HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
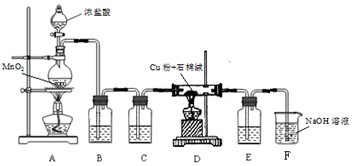
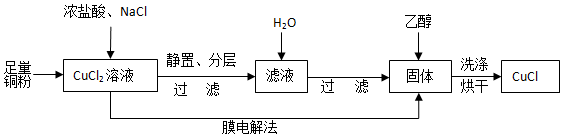
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
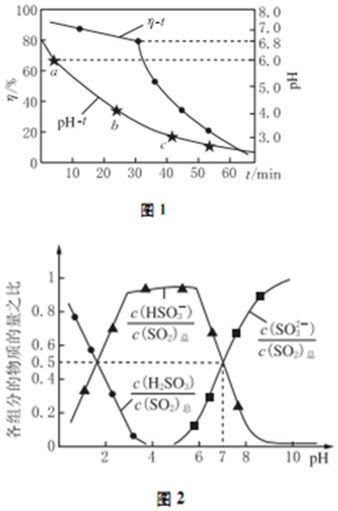
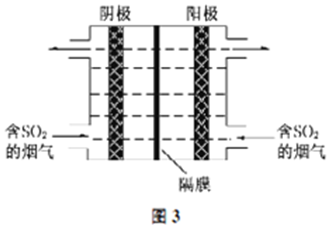
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①表示2molC(s)燃烧生成2molCO(g)需要吸收221 kJ的热量 | |
| B. | 碳的燃烧热大于110.5 kJ/mol | |
| C. | 稀硫酸与浓NaOH溶液反应的中和热为-57.3 kJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com