
下列各种情况下,常温下溶液中一定能大量存在的离子组是
A.由水电离出的c(H+)=l×10-12mol/L的溶液中:K+、Ba2+、Cl-、NO3-
B.无色溶液中可能大量存在 : Al3+、NH4+、Cl﹣、S2﹣
C.pH=7的中性溶液中:Fe3+、K+、Cl-、SO42-
D.酸性溶液中可能大量存在 : Na+、ClO﹣、SO42﹣、CN﹣
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
下列对 H2(g)+
H2(g)+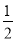 I2(g)===HI(g)ΔH=+26 kJ·mol-1的叙述中,正确的是
I2(g)===HI(g)ΔH=+26 kJ·mol-1的叙述中,正确的是
A.1 mol氢气和1 mol碘蒸气完全反应需要吸收26 kJ的热量
B.1个氢分子和1个碘分子完全反应需要吸收52 kJ的热量
C.1 mol H2(g)与1 mol I2(g)完全反应生成2 mol的HI气体需吸收52 kJ的热量
D.1 mol H2(g)与1 mol I2(g)完全反应放出26 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三9月月考化学试卷(解析版) 题型:选择题
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是
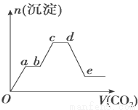
A.Oa段反应的化学方程式是Ba(OH)2+CO2═BaCO3↓+H2O
B.ab段与cd段所发生的反应相同
C.de段沉淀减少是由于BaCO3固体消失
D.bc段反应的离子方程式是2AlO2﹣+3H2O+CO2═2Al(OH)3↓+CO32﹣
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期入学考试化学试卷(解析版) 题型:选择题
海水开发利用的部分过程如图所示。下列说法错误的是
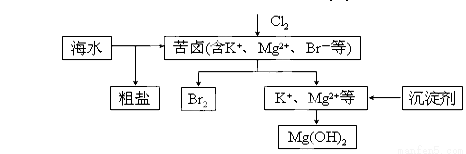
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产中常选用N aOH作为沉淀剂
aOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源:2016届贵州省遵义市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列是某学生提供的实验数据及操作,以下组合中,完全正确的是
①配制480mL0.1mol/L氢氧化钠溶液用500mL的容量瓶;②用托盘天平称取5.85gNaCl固体;③中和滴定操作时,消耗0.1000mol/L的盐酸 23.0mL;④用广泛pH试纸测得血液的pH=7.4;⑤实验室用乙醇制乙烯时,为更好控制温度选择水浴加热法
A.只有①正确 B.只有②错误
C.①③④正确 D.①②③④⑤全错
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省高二上化学试卷(解析版) 题型:选择题
某锂电池的电池总反应为4Li+2SOCl2=4LiCl+S+SO2,下列有关说法正确的是
A.锂电极作电池负极,放电过程中发生还原反应
B.1 mol SOCl2发生电极反应转移的电子数为4 mol
C.电池的正极反应为2SOCl2+2e-=4Cl-+S+SO2
D.组装该电池必须在无水、无氧的条件下进行
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁葫芦岛一中高二上期初考试化学试卷 (解析版) 题型:选择题
NA表示阿伏加德罗常数,下列说法正确的是
A.2.7 g铝与足量的NaOH溶液反应,转移的电子总数为NA
B.1 mol Al分别放入足量的冷的浓HNO3、稀HNO3中,反应后转移的电子均为3NA个
C.各5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA
D.1 mol Na与足量O2反应生成Na2O或Na2O2均失去NA个电子
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三上学期第一次月考化学试卷(解析版) 题型:填空题
(14分)氮和硫的化合物对大气都有严重污染,据所学化学反应原理回答下列问题:
(1)NO2与悬浮在大气中海盐粒子的相互作用时发生反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) ∆H = a KJ/mol
NaNO3(s)+ClNO(g) ∆H = a KJ/mol
则该反应为 反应(填放热或吸热),产物ClNO的结构式为 。
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为 (已知HNO2的电离常数Ka=7.1×10-4mol/L,CH3COOH的电离常数K a=1.7×10-5mol/L,可使溶液A和溶液B的pH相等的方法是 。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)若将SO2,NO2,O2按4:4:3通入水中充分反应,写出总的离子方程式 。
(4)向氨水中通入过量的H2S,所得溶液M中溶质的电子式为 ;取0.2mol/L的NaOH溶液与0.1mol/L的M溶液等体积混合,加热至充分反应后,待恢复至室温,剩余溶液中离子浓度由大到小的顺序是 ,此时测得溶液的pH=12,则此条件下M溶液中阴离子的电离平衡常数Ka= (提示:若涉及多元弱酸的电离或多元弱酸根离子的水解,均只考虑第一步电离或水解)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省太原市高一上入学考试化学试卷(解析版) 题型:选择题
除去下列物质中的少量杂质,所用方法正确的是( )
选项 | 物质(括号内为杂质) | 除去杂质的方法 |
A | KCl(MnO2) | 加水溶解,过滤,洗涤,干燥 |
B | FeSO4溶液(CuSO4) | 加入适量的锌粉,过滤 |
C | NaCl溶液(CuCl2) | 加入过量的NaOH溶液,过滤 |
D | O2(H2O) | 将混合气体通过盛有足量浓硫酸的洗气瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com