
| A. | 冰醋酸中醋酸分子之间 | |
| B. | 可燃冰(CH4•8H2O)中甲烷分子与水分子之间 | |
| C. | 液态氟化氢中氟化氢分子之间 | |
| D. | 一水合氨分子中的氨分子与水分子之间 |
科目:高中化学 来源: 题型:选择题
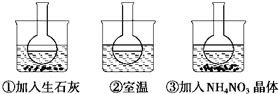
| A. | 氯化钠溶解度减小 | B. | 溶液中溶质的质量分数变小 | ||
| C. | 溶剂的质量减小 | D. | 溶液变成不饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 普通水泥 | B. | 普通玻璃 | C. | 汽车轮胎 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2是气体,SiO2是固体 | |
| B. | 二氧化硅的熔点比二氧化碳高 | |
| C. | CO2溶于水形成碳酸,SiO2难溶于水 | |
| D. | CO2通入Na2SiO3溶液中析出硅酸沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
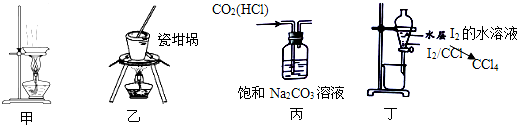
| A. | 甲用装置所示仪器可以蒸发、结晶制取粗盐 | |
| B. | 用装置乙加热分离碘单质和氯化钠的混合固体 | |
| C. | 用装置丙除去CO2中的少量HCl | |
| D. | 用装置丁进行萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液变红 | |
| B. | Na2O与Na2O2组成元素相同、阴阳离子个数比相同,但跟水反应的产物不同 | |
| C. | 只存在共价键的物质一定是共价化合物、离子化合物中一定含有离子键 | |
| D. | 难溶电解质AB2的饱和溶液中,c(A2+)=xmol•L-1,c(B-)=y mol•L-1,则Ksp值为4xy2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论 | |
| A | 切开金属钠,钠表面的银白色会逐渐褪去 | Na在空气中会生成Na2O2 |
| B | 向某溶液中滴加BaCl2溶液,出现白色沉淀,再加足量稀HCl,若白色沉淀不溶解 | 原溶液中一定含SO42- |
| C | 向Fe(NO3)2溶液中滴加稀硫酸和KSCN溶液,变成红色 | 溶液中有Fe3+生成 |
| D | 将FeCl2溶液滴加到少许酸性KMnO4溶液中,溶液褪色 | FeCl2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com