
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.100g质量分数为17%的H2O2水溶液中含氧原子数目为NA
B.0.1molH2(g)与0.1molI2(g)于密闭容器中充分反应生成HI(g)后,其分子总数小于0.2NA
C.8.0gCH4与足量Cl2在光照下反应生成的HCl分子数最多为2NA
D.标准状况下,将54g铝片投入足量冷的浓硝酸中生成134.4LNO2
【答案】C
【解析】
A.100g质量分数为17%的双氧水,其中H2O2的质量为17g,即0.5mol,仅H2O2中就含有1NA个氧原子,此外,还有83g水中含有的氧原子未计入,A项错误;
B.H2与I2的反应方程式为:![]() ,反应前后分子总数不变,所以0.1molH2与0.1molI2混合后反应,容器内分子数始终为0.2NA,B项错误;
,反应前后分子总数不变,所以0.1molH2与0.1molI2混合后反应,容器内分子数始终为0.2NA,B项错误;
C.CH4与Cl2在光照下发生取代反应,每有一个CH4中的H原子被Cl原子取代,同时就会生成一个HCl分子,8.0gCH4即0.5mol,总共含有2NA个H原子,所以最多可以生成2NA个HCl分子,C项正确;
D.铝遇到冷的浓硝酸或浓硫酸均会发生钝化现象,只是Al的表层被氧化为致密的Al2O3薄膜,而内部的Al得到有效地保护,无法被氧化,D项错误;
答案选C。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】Fe3O4中含有Fe(Ⅱ)、Fe(Ⅲ),以Fe3O4/Pd为催化材料,可实现用H2消除酸性废水中的致癌物NO2-,其反应过程如图所示。下列说法正确的是( )
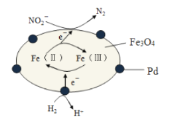
A.Pd作正极
B.Fe(Ⅱ)与Fe(Ⅲ)的相互转化起到了传递电子的作用
C.反应过程中NO2-被Fe(Ⅱ)氧化为N2
D.用该法处理后水体的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列有关说法正确的是
A.60克的乙酸和葡萄糖混合物充分燃烧消耗O2分子数为2NA
B.5.8g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.04NA
C.把4.6g乙醇完全氧化变成乙醛,转移电子数为0.1NA
D.实验室制取氧气方法有多种,制取1molO2转移电子数均是4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,向10 mL 0.1 mol/L CuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中-lg c(Cu2+)与Na2S溶液体积的关系如图所示.下列有关说法正确的是( )

A.0.1mol/LNa2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
B.a、b、c三点对应的溶液中,水的电离程度最大的为b点
C.该温度下,Ksp(CuS)的数量级为10-36
D.向10 mL Ag+、Cu2+物质的量浓度均为0.1mol/L的混合溶液中逐滴加入0.01mol/L的Na2S溶液,Cu2+先沉淀[已知:Ksp(Ag2S)=6.4×10-50]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是________,基态D原子价电子的轨道表达式为________________。
(2)DA2分子的VSEPR模型是____________。
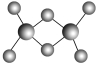
(3)实验测得C与氯元素形成的化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
①C2Cl6属于________(填晶体类型)晶体,其中C原子的杂化轨道类型为________杂化。
②[C(OH)4]-中存在的化学键有____________________________________________。
(4)单质A有两种同素异形体,其中沸点高的是__________ (填分子式),原因是______________________________________________________________
(5)D与E所形成化合物晶体的晶胞如图所示 。
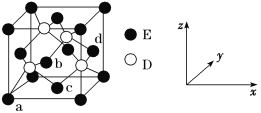
①在该晶胞中,E的配位数为________。
②原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2);c为(1/2,1/2,0)。则d的坐标参数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应均可获取H2。下列有关说法正确的是()
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=+571.6kJ/mol
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ/mol
A.反应①中电能转化为化学能
B.反应②为放热反应
C.反应CH4(g)═C(s)+2H2(g)的△H=74.8kJ/mol
D.反应③使用催化剂,△H3不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0.0200mol/L稀盐酸滴定20.00mL0.0200mol/LNaY溶液,溶液中水的电离程度随所加稀盐酸的体积变化如图所示(忽略滴定过程中溶液的体积变化或密度变化),则下列有关说法正确的是()
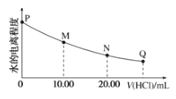
已知:K(HY)=5.0×10-11
A.M点溶液的pH>7
B.M点,c(Na+)=c(HY)+c(Y-)+c(Cl-)
C.可选取酚酞作为滴定指示剂
D.图中Q点水的电离程度最小,Kw<10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某配位化合物为深蓝色晶体,由原子序数由小到大的A,B,C,D,E五种元素组成,其原子个数比为14∶4∶5∶1∶1。其中C,D同主族且原子序数D为C的2倍,E元素的外围电子排布式为(n-1)dn+6ns1,试回答下列问题:
(1)元素B,C,D的第一电离能由大到小排列顺序为________(用元素符号表示)。
(2)D元素基态原子的最外层电子排布图为________。
(3)该配位化合物的化学式为________,配体的中心原子的杂化方式为________。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可以任意比互溶,解释其主要原因为_______________。
(5)A元素与B元素可形成分子式为B2A2的某化合物,该化合物的分子具有平面结构,则其结构式为________,分子中含有________个σ键,________个π键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】七水合硫酸镍为水绿色斜方棱形晶体,有甜味,俗称“翠矾”。某学习小组用含镍催化剂废渣(主要成分是镍单质,含少量铁、铝单质及其氧化物,以及少量难溶性杂质),制备七水合硫酸镍晶体,流程图如下:
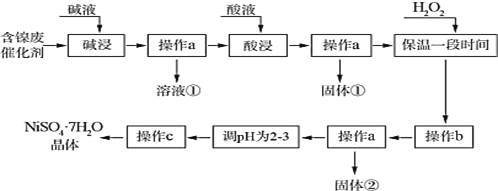
几种难溶碱开始沉淀和完全沉淀的 pH:
沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀 | 3.8 | 2.7 | 7.6 | 7.1 |
完全沉淀 | 5.2 | 3.2 | 9.7 | 9.2 |
回答下列问题:
(1)“碱浸”操作发生的离子方程式为____________。
(2)①“固体①”的主要成分是__________,双氧水作用为___________。
②如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是_______________________,设计实验证明产品中是否含“杂质”:____________。(不考虑硫酸镍影响)
(3) “操作 b”中调节溶液 pH 范围是_________,“操作 c”之前,“调节 pH 为 2~3”的目的是_______。
(4) “操作 c”具体是指___________________、过滤、洗涤、干燥。
(5)取 4.000 g 硫酸镍晶体产品(NiSO4·7H2O)于锥形瓶中,加入足量的去离子水溶解,用0.2000 mol·L-1 的标准溶液EDTA(Na2H2Y)滴定至终点(发生Ni2++ H2Y2- = NiY2-+ 2H+ ),三次实验消耗标准液的体积分别为 69.10 mL、68.90 mL、59.00 mL,则产品纯度为_________%。(计算结果保留到小数点后 2 位,不考虑杂质反应)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com