
分析 (1)强电解质完全电离,电离方程式用“=”,弱电解质部分电离,电离方程式用“?”,电离遵循电荷守恒和质量守恒定律,并注意酸根离子等原子团不可拆分,以此来解答;
(2)①氯化铵在溶液中电离出铵根离子,铵根离子结合水电离的氢氧根离子生成一水合氨和氢离子;
②在溶液中铝离子水解生成氢氧化铝胶体,具有较强吸附性,从而能够净水;
③用NaHCO3与Al2(SO4)3两种溶液分别水解呈碱性和酸性,可发生互促水解生成氢氧化铝沉淀和二氧化碳气体;
(3)根据溶度积表达式为离子的浓度的幂次方之积来进行书写;
(4)①钢铁发生吸氧腐蚀的正极氧气得到电子;
②燃料电池的分解氢气失去电子生成氢离子;
③用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气.
解答 解:(1)①H2S是二元弱酸,属弱电解质,分两步电离,第一步电离出氢离子和硫氢根离子,第二步电离:硫氢根离子电离出硫离子和氢离子,其电离方程式为:H2S?H++HS-、HS-?H++S2-,
故答案为:H2S?H++HS-、HS-?H++S2-;
②碳酸氢钠为强电解质,在水溶液中完全电离出钠离子和碳酸氢根离子,注意碳酸氢根离子为弱酸的酸式根离子,不能拆,电离方程式为:NaHCO3═Na++HCO3-,
故答案为:NaHCO3═Na++HCO3-;
③NaHSO4是强酸强碱酸式盐,属强电解质,完全电离,电离出Na+、H+、SO42-离子,其电离方程式为:NaHSO4=Na++H++SO42-,
故答案为:NaHSO4=Na++H++SO42-;
(2)①铵根离子在溶液中水解生成一水合氨和氢离子,水解方程式为:NH4++H2O?NH3•H2O+H+,
故答案为:NH4++H2O?NH3•H2O+H+;
②明矾为硫酸铝钾,在溶液中硫酸铝钾电离出铝离子,铝离子水解生成氢氧化铝胶体,Al3++3H2O?Al(OH)3(胶体)+3H+,氢氧化铝胶体具有较强吸附性,从而能够净水,
故答案为:Al3++3H2O?Al(OH)3(胶体)+3H+;
③用NaHCO3与Al2(SO4)3两种溶液分别水解呈碱性和酸性,可发生互促水解,可做泡沫灭火剂,反应的离子方程式为:3HCO3-+Al3+=3CO2↑+Al(OH)3↓,
故答案为:3HCO3-+Al3+=3CO2↑+Al(OH)3↓;
(3)溶度积表达式为离子的浓度的幂次方之积,所以Mg(OH)2的溶度积表达式是:Ksp=c(Mg2+)•c(OH-)2,
故答案为:Ksp=c(Mg2+)•c(OH-)2;
(4)①钢铁发生吸氧腐蚀的正极反应式为:O2+4e-+2H2O═4OH-,
故答案为:O2+4e-+2H2O═4OH-;
②酸性溶液中负极氢气失去电子生成氢离子,电极反应为:2H2-4e-=4H+,
故答案为:2H2-4e-=4H+;
③用惰性电极电解饱和食盐水时,阳极上氯离子放电生成氯气、阴极上氢离子放电生成氢气,电池反应式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑,
故答案为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑.
点评 本题考查了离子方程式、盐的水解原理、电极反应式、化学方程式的书写,题目难度中等,试题知识点较多、题量较大,充分考查了学生的分析能力及灵活应用能力,注意掌握书写离子方程式、化学方程式的原则,明确电解原理、原电池原理及水解原理.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至Ba2+恰好完全沉淀 | |
| B. | 向NaHSO4溶液中.逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀 | |
| C. | 向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量 | |
| D. | 向pH=1的NaHSO4溶液中加入等体积pH=13的Ba(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
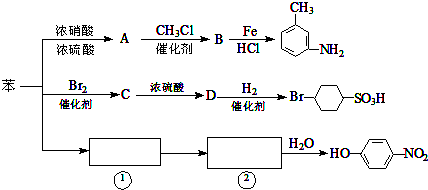
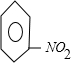 +CH3Cl$\stackrel{催化剂}{→}$
+CH3Cl$\stackrel{催化剂}{→}$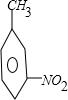 +HCl.
+HCl. ,②
,② 或
或 .
.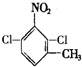 、
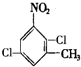
、
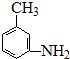 的所有原子不是(填“是”或“不是”)在同一平面上.
的所有原子不是(填“是”或“不是”)在同一平面上.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2A12O3+3C $\frac{\underline{\;高温\;}}{\;}$A1+3CO2↑ | B. | MgO十H2$\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O | ||
| C. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | D. | 2HgO$\frac{\underline{\;电解\;}}{\;}$2Hg+O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只用一种试剂就可以鉴别乙醇、乙酸、四氯化碳、苯四种液体 | |
| B. | 乙醇、乙醛、乙酸都易溶于水,都能与金属钠反应放出氢气? | |
| C. | 糖类、油脂、蛋白质是重要的营养物质,都能发生水解反应? | |
| D. | 甲烷、乙烯和苯都可以从石油中提取,都能使溴水褪色? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com