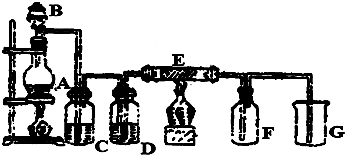
A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间有如图所示的反应关系(反应物和生成物均无省略),反应①②均是工业生产中的重要反应.
请回答下列问题:
(1)A的化学式为
,电解时的阳极电极反应式为
(2)反应①的化学方程式是
在2L密闭容器中,800℃时反应2C(g)+甲(g)═2D(g)体系中,n(C)随时间的变化如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(C)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(3)写出该反应的平衡常数表达式:K=
(用具体物质表示),已知:K(300℃)>K(350℃),该反应是
反应(填“放热”或“吸热”); 0~2s内该反应的平均速率v(甲)=
(4)能说明该反应已经达到平衡状态的是
a.v(D)=2v(甲)
b.容器内压强保持不变
c.v逆(C )=2v正(甲)
d.容器内物质的密度保持不变
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.即时分离出D 气体b.适当升高温度c.增大甲的浓度d.通入惰性气体增加压强
(6)某温度下,容积均为1L的两个密闭容器中均进行:2C(g)+甲(g)═2D(g),某时刻各物质的物质的量(mol)及正逆反应速率关系如下表所示:
| 容器编号 | n(甲) | n(C) | n (D) | v正与v逆的关系 |
| Ⅰ | 0.20 | 0.10 | 0.20 | v正=v逆 |
| Ⅱ | 0.20 | 0.40 | 1.00 | ②? |
填写表中空格:②
.

 A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间有如图所示的反应关系(反应物和生成物均无省略),反应①②均是工业生产中的重要反应.
A、B、C、D都是中学化学中的常见化合物,均由周期表前18号元素组成,D为红综色气体,甲、乙则是两种单质,以上单质和化合物之间有如图所示的反应关系(反应物和生成物均无省略),反应①②均是工业生产中的重要反应.


 经两步反应制得,写出第一步反应的化学方程式
经两步反应制得,写出第一步反应的化学方程式