
下列有关说法正确的是
| A.实验室制氢气,为了加快反应速率,可向稀H2SO4;中滴加少量Cu(NO3)2溶液 |
| B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
C.反应N2(g)+3H2(g) 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大 |
| D.吸热反应“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 |
B
解析试题分析:Cu(NO3)2溶液在酸性条件下具有强氧化性,与金属反应不生成氢气,故A错误;CaSO4是一种强酸强碱盐,碳酸钙为弱酸强碱盐,工业上用Na2CO3溶液浸泡锅炉水垢使其中CaSO4能转化为CaCO3,因为CaSO4溶解度大于CaCO3,这样使水垢疏松,易于处理,B选项正确;反应N2(g)+3H2(g) 2NH3(g)△H<0平衡时,其他条件不变,升高温度,逆向移动,氢气转化率减小,C选项错误;反应自发进行的判断依据是△H-T△S<0,反应自发进行,△H-T△S>0,反应非自发进行;据此判断“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”反应的△H>0,△S<0,则△H-T△S>0,反应一定非自发进行,D选项错误。
2NH3(g)△H<0平衡时,其他条件不变,升高温度,逆向移动,氢气转化率减小,C选项错误;反应自发进行的判断依据是△H-T△S<0,反应自发进行,△H-T△S>0,反应非自发进行;据此判断“TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)”反应的△H>0,△S<0,则△H-T△S>0,反应一定非自发进行,D选项错误。
考点:考查了化学基本理论的知识。


科目:高中化学 来源: 题型:单选题
反应mA(g)+ nB(g)  pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3 mol/L,又测得平均反应速率v(C)=2v(B)。达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为( )
pC(g)+qD(g),经5min后达到平衡,测得此时A的浓度减少了a mol/L,同时C的浓度增加了2a/3 mol/L,又测得平均反应速率v(C)=2v(B)。达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为( )
A.2A(g)+ 6B(g) 3C(g)+5D(g)
3C(g)+5D(g)
B.3A(g)+ B(g) 2C(g)+2D(g)
2C(g)+2D(g)
C.3A(g)+ B(g)  2C(g)+ D(g)
2C(g)+ D(g)
D.A(g)+ 3B(g) 2C(g)+2D(g)
2C(g)+2D(g)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定温度下,可逆反应2A(g)+3B(g)  2C(g)达到平衡的标志是( )。
2C(g)达到平衡的标志是( )。
A.A的生成速率与C的分解速率相等
B.单位时间生成2n mol A,同时生成3n mol B
C.A、B、C的浓度不再变化
D.A、B、C的分子数之比为2∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在某恒容密闭容器中进行如下可逆反应:2M(g)+N(g)  W(?)+4Q(g) ΔH<0,起始投料只有M和N。下列示意图正确且能表示该可逆反应达到平衡状态的是( )
W(?)+4Q(g) ΔH<0,起始投料只有M和N。下列示意图正确且能表示该可逆反应达到平衡状态的是( )
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:
2SO2(g)+O2(g)  2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s | 0 | t1 | t2 | t3 | t4 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知反应①:CO(g)+CuO(s)??CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)  Cu(s)+H2O(g)在相同温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1= |
| B.反应③的平衡常数K=K1/K2 |
| C.对于反应③,恒容时,若温度升高,H2的浓度减小,则该反应的焓变为正值 |
| D.对于反应③,恒温恒容时,若增大压强,H2的浓度一定减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
利用反应:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH ="+746.8" kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是 ( )
2CO2(g)+N2(g) ΔH ="+746.8" kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是 ( )
| A.降低温度 |
| B.增大压强同时加催化剂 |
| C.升高温度同时充入N2 |
| D.及时将CO2和N2从反应体系中移走 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究。T1℃时,将9 mol CO2和12 mol H2充入3 L密闭容器中,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
| A.曲线Ⅱ对应的条件改变是增大压强 |
| B.T2℃时,上述反应平衡常数为0.42,则T2>T1 |
| C.在T1℃,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和5 mol H2O(g),则达平衡前v(正)>v(逆) |
D.在T1℃,若起始时向容器充入4.5 mol CO2、6 mol H2,平衡时容器内压强p= |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为了变废为宝,控制温室效应,工业上可用CO2来生产甲醇。一定条件下发生如下反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)。如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。
CH3OH(g)+H2O(g)。如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。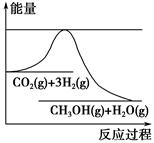
| A.降低温度 |
| B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离出来 |
| D.再充入1 mol CO2和3 mol H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com