
分析 ①维生素A又称视黄醇,为脂溶性维生素,缺乏维生素A会患夜盲症;
②a.复方氢氧化铝片属于治疗胃酸过多的药物; b.阿司匹林为解热镇痛药,不属于抗生素;c.青霉素属于抗生素;
③加碘盐中加入的是碘酸钾;
④在食品加工或餐饮业中,特别要严加控制用量的物质是亚硝酸盐;
⑤地沟油的主要成分是高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油,据此解答即可.
解答 解:①维生素A又称视黄醇,为脂溶性维生素,缺乏维生素A会患夜盲症,故答案为:c;
②a.复方氢氧化铝片属于治疗胃酸过多的药物,不属于抗生素;
b.阿司匹林为解热镇痛药,不属于抗生素;
c.青霉素属于抗生素;
故选c;
③加碘盐中加入的是碘酸钾,故答案为:b;
④亚硝酸盐在人体内特定条件下回生成亚硝铵,亚硝铵属于致癌物质,因此在食品加工或餐饮业中,特别要严加控制用量的物质是亚硝酸钠,故答案为:a;
⑤地沟油的主要成分是高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油,故答案为:甘油.
点评 本题主要考查的是维生素与人体健康、抗生素药物识别、碘盐中的成分、酯类的水解等,综合性较强,体现了化学来源于生活、服务于生活的宗旨,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 将pH试纸直接放入某溶液中,测定该溶液的pH | |
| B. | 用澄清石灰水鉴别NaHCO3和Na2CO3 | |
| C. | 过滤操作时,漏斗下部的尖嘴要紧靠烧杯的内壁 | |
| D. | 从碘水提取碘可用乙醇作萃取剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
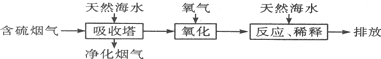
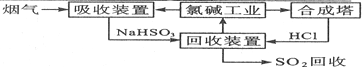
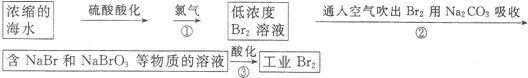
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


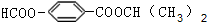 .
.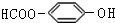 . (写结构简式)
. (写结构简式)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| W | Z |
| A. | X、Y、Z三种元素最低价氢化物的沸点依次升高 | |
| B. | 由X、Y和氢三种元素形成的化合物中只有共价键 | |
| C. | 物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 | |
| D. | X的阴离子比Y的阴离子离子半径大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
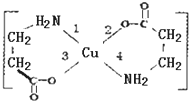 II.二甘氨酸合铜(II)是最早被发现的电中性内配盐,它的结构如图:
II.二甘氨酸合铜(II)是最早被发现的电中性内配盐,它的结构如图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
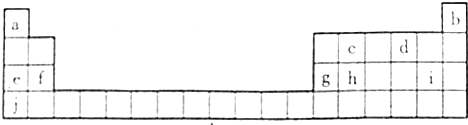
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com