
A.SO2+H2O H2SO3 H2SO3 |
| B.SO2+2NaOH=Na2SO3+H2O |
C.2SO2+O2 2SO3 2SO3 |
| D.SO2+CaO=CaSO3 |
科目:高中化学 来源:不详 题型:单选题
| A.①②④ | B.②③⑤ | C.②④⑤⑥ | D.①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜与稀硫酸,铜与浓硫酸 |
| B.铁与稀硫酸,铁与浓硫酸 |
| C.硫化钠与稀硫酸,亚硫酸钠与稀硫酸 |
| D.硫化钠与稀硫酸,硫化钠与稀盐酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.Ba(NO3)2 | B.BaCl2 | C.Ba(OH)2 | D.溶有NH3的BaCl2溶液 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
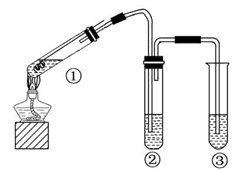
| A.上下移动①中铜丝可控制SO2的量 |
| B.②中选用品红溶液验证SO2的生成 |
| C.③中选用NaOH溶液吸收多余的SO2 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙 |
B.反应Ⅲ中发生反应的化学方程式为CaSO4+4C  CaS+4CO↑ CaS+4CO↑ |
| C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解 |
| D.反应Ⅴ中的副产物氯化铵可用作氮肥 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
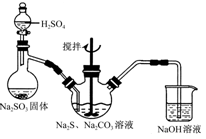
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶1 | B.1∶2 | C.2∶3 | D.4∶3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
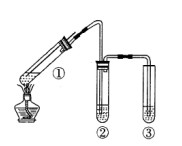
| A.上下移动①中铜丝可控制SO2的量 |
| B.②中选用品红溶液验证SO2的生成 |
| C.③中选用NaOH溶液吸收多余的SO2 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com