
A、 用酒精萃取溴水中的溴 |
B、 将硫酸铜溶液直接蒸干得到胆矾 |
C、 说明2NO2(g)?N2O4(g)△H<0 |
D、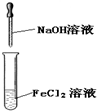 实验室制备Fe(OH)2 |


 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:
| A、电解饱和食盐水的阳极反应:2H2O+2e-=H2↑+2OH- | ||
B、碳酸钠溶液呈碱性的原因:CO
| ||
C、向AgNO3溶液中加入过量氨水:Ag++NH3?H2O=AgOH↓+NH
| ||
D、泡沫灭火器反应原理:A12++3HCO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 草酸亚铁(FeC2O4)常用作分析剂、显影剂以及新型电池材料磷酸亚铁锂的生产.
草酸亚铁(FeC2O4)常用作分析剂、显影剂以及新型电池材料磷酸亚铁锂的生产.查看答案和解析>>
科目:高中化学 来源: 题型:
 镓(Ga)、锗(Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途.试回答下列问题:
镓(Ga)、锗(Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气象环境报告中的“PM2.5”是对一种新分子的描述 |
| B、地沟油的主要成分是油脂,其组成与汽油、煤油不相同 |
| C、“玉兔号”月球车太阳能电池帆板的材料是二氧化硅 |
| D、高铁车厢采用的铝合金材料强度大、质量轻,不与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、风力发电 | B、汽车尾气 |
| C、煤炭燃烧 | D、建筑扬尘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.5 mol Fe2+与含0.5 mol H2O2溶液反应,转移NA个电子(NA表示阿伏加德罗常数) | ||
B、常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中
| ||
| C、复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是2 Fe3++3SO42-+3Ba2++6 OH-=3BaSO4↓+2Fe(OH)3↓ | ||
| D、向2mL 0.1mol/L的硝酸银溶液中滴加几滴0.1mol/L氯化钠溶液,产生白色沉淀,再滴加几滴硫化钠溶液,产生黑色沉淀,说明氯化银能转化为更难溶的硫化银 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、装置①可用于已知浓度的氢氧化钠溶液测定未知浓度盐酸的实验 |
| B、装置②可用于氯化铵固体和氢氧化钙固体反应制取少量氨气 |
| C、装置③可用于收集SO2,并吸收多余的SO2 |
| D、装置④可用于制取少量Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com