
【题目】下列关于燃烧热的说法中正确的是( )
A.燃烧热是指1mol物质燃烧所放出的热量
B.燃烧热是指常温下,可燃物燃烧放出的热量
C.燃烧热是指1.01×105Pa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量
D.燃烧热随化学计量数的改变而改变
科目:高中化学 来源: 题型:
【题目】【上海市闵行区2017届高三上学期期末教学质量调研(一模)化学试题】利用海水可以提取氯化钠、溴、碘等产品。海带提碘的流程如下:
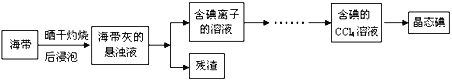
(1)CCl4含有___________键的______________分子(均选填“极性”或“非极性”)。
(2)灼烧海带时除需要三脚架、酒精灯、泥三角外,还需要的主要仪器是____________。
(3)为更好的完成实验,灼烧海带时,需加入一定量的氢氧化钠充分混合后再灼烧。此操作目的是___________________________________。
(4)向盛有碘离子溶液中加入CCl4和氯水,______(填:“上”或“下”)层呈紫红色;如果氯水加过量,CCl4层会由紫红色变成无色。整个过程中被氧化的微粒是__________________。写出并配平CCl4层由紫红色变成无色的化学反应方程式:__________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 人体从食物中摄取的营养物质都是有机物
B. 75%和95%的医用酒精都可直接用于杀菌消毒
C. 蔗糖和麦芽糖的水解产物不完全相同
D. 有机物在空气中都可以燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.24 g淀粉与3.42 g蔗糖的混合物加水后,在一定条件下充分水解,所得溶液中葡萄糖与果糖的质量之比为( )
A. 1:1 B. 3:1 C. 4:1 D. 1:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,ΔH1=-393.5kJ·mol-1,ΔH2=-395.4kJ·mol-1,
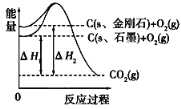
下列说法或表示式正确的是
A.石墨和金刚石的转化是物理变化
B.C(s、石墨)===C(s、金刚石)ΔH =+1.9kJ·mol-1
C.金刚石的稳定性强于石墨
D.断裂1mol石墨的化学键吸收的能量比断裂1mol金刚石的化学键吸收的能量少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017届宁夏六盘山高级中学高三上月考二化学卷】研究NOx、CO等大气污染物的测量及处理具有重要意义。
(1)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。NOx在催化转化器中被CO还原成N2排除。写出NO被CO还原的化学方程式:________________。
(2)选择性催化还原技术(SCR)是目前最成熟的烟气脱硝技术,即在金属催化剂作用下,用还原剂(如NH3)选择性地与NOx反应生成N2和H2O。
①已知:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)△H=-905.5kJmol-1
4NO(g)+6H2O(g)△H=-905.5kJmol-1
N2(g)+O2(g)![]() 2NO(g)△H=+180kJmol-1
2NO(g)△H=+180kJmol-1
完成该方法中主要反应的热化学方程式
4NH3(g)+4NO(g)+O2(g)![]() 4N2(g)+6H2O(g)△H=_________________。
4N2(g)+6H2O(g)△H=_________________。
②该方法应控制反应温度在315~400℃之间,反应温度过低会影响反应速率,但温度也不宜过高,原因是___________________。
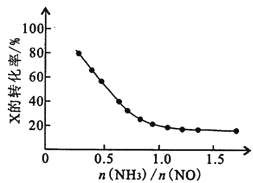
③氨氮比[n(NH3)/n(NO)]会直接影响该方法的脱硝率。350℃时,只改变氨气的投放量,反应物x的转化率与氨氮比的关系如图所示,则X是________________ (填化学式)。当n(NH3)/n(NO)>1.0时,烟气中NO浓度反而增大,主要原因是________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在科研与生活中有重要作用,某兴趣小组用0.50mol/L KI、0.2%淀粉溶液、0.10molL﹣1K2S2O8、0.20molL﹣1Na2S2O3等试剂,探究反应条件对化学反应速率的影响.
已知:S2O82﹣+2I﹣=2SO42﹣+I2(慢) I2+2S2O32﹣=2I﹣+S4O62﹣ (快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的_________耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,Na2S2O3与K2S2O8初始的体积v(Na2S2O3)与v(K2S2O8)量需满足的关系为:v(Na2S2O3)______v(K2S2O8)(填“>”,“<”,“=”),出现蓝色之前,I-在反应中起到的作用是_________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/ml | 出现蓝色的时间t/s | ||||
K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | ||
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 | 10 |
② | 5.0 | V1 | 4.0 | 4.0 | 2.0 | 20 |
③ | 10.0 | V2 | 2.0 | 4.0 | 2.0 | 20 |
④ | 10.0 | V3 | 4.0 | 2.0 | 2.0 | 5 |
①表中V1________,V2_______,V3=______ .
②用K2S2O8表示实验序号①、②、④的速率分别为_____mol·L-1·s-1.
③根据实验结构,以下说法正确的有_____
A.该反应的速率与K2S2O8的浓度成正相关
B.该反应的速率与KI的浓度成正相关
C.该反应的速率与Na2S2O3的浓度成正相关
D.多步反应的速率由慢速反应速率决定
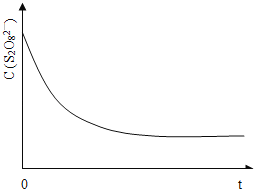
(3)已知某条件下,浓度c(S2O82﹣)随反应时间t的变化曲线如图,若保持其它条件不变,图中,分别画出降低反应温度和加入催化剂时c(S2O82﹣)随反应时间t的变化曲线示意图(进行相应的标注)_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【江苏省镇江市2017届高三三模(最后一卷)化学试题】以熔融Na2CO3为电解质,H2和CO混合气为燃料的电池原理如下图所示。
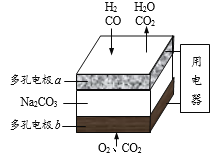
下列说法正确的是
A. b是电池的负极
B. a电极的反应为:CO+CO32ˉ-2eˉ== 2CO2;H2+CO32ˉ-2eˉ== H2O+CO2
C. a电极上每消耗22.4L原料气,电池中转移电子数约为2╳6.02╳1023
D. a、b两极消耗的气体的物质的量之比是1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【福建省福州第一中学2017届高三5月质检(最后一模)理综化学试题】
下图所示原电池的总反应为Cu(s)+2Ag+(aq)![]() Cu2+(aq)+2Ag(s),下列叙述正确的是
Cu2+(aq)+2Ag(s),下列叙述正确的是
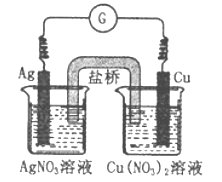
A. 电子从银电极经导线流向铜电极
B. 工作一段时间后,右烧杯中溶液的pH变小
C. 电池工作时,Cu2+向铜电极移动
D. 将AgNO3溶液更换为Fe(NO3)3溶液,电流计指针反向偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com