
���� ��1��������Ũ�ȵ���֮���뷴Ӧ��Ũ�ȵ���֮��֮��Ϊƽ�ⳣ�����Դ˿�ȷ����ѧ����ʽ��
��2����427��ʱ��CO ��H2O��g����0.01molͨ�����Ϊ2�����ܱ������з�Ӧ��5����ʱ�ﵽƽ��״̬���÷�Ӧ��ƽ�ⳣ����9����CO��ת������x��������ʽ��ʽ�õ���
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 0.01 0.01 0 0
�仯����mol�� 0.01x 0.01x 0.01x 0.01x
ƽ������mol��0.01-0.01x 0.01-0.01x 0.01x 0.01x
���ƽ�ⳣ���ɼ���CO��ת���ʣ�
��� �⣺��1����K=$\frac{c��CO��•C��{H}_{2}��}{c��{H}_{2}O��}$��֪����Ӧ��ΪC��H2O��������ΪCO��H2���÷�ӦΪC��s��+H2O��g��?CO��g��+H2��g����
�ʴ�Ϊ��C��s��+H2O��g��?CO��g��+H2 ��g����
��2����427��ʱ��CO ��H2O��g����0.01molͨ�����Ϊ2�����ܱ������з�Ӧ��5����ʱ�ﵽƽ��״̬���÷�Ӧ��ƽ�ⳣ����9����CO��ת������x��������ʽ��ʽ�õ���
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 0.01 0.01 0 0
�仯����mol�� 0.01x 0.01x 0.01x 0.01x
ƽ������mol��0.01-0.01x 0.01-0.01x 0.01x 0.01x
K=$\frac{��0.01x��^{2}}{��0.01-0.01x��^{2}}$=9��
x=0.75=75%��
�ʴ�Ϊ��75%��
���� ���⿼���˻�ѧƽ��ļ�����ƽ�ⳣ����ת���ʵ�֪ʶ�ļ���Ӧ�ã�Ϊ��Ƶ���㣬���ؿ���ѧ���ķ���������������ע�����ƽ�ⳣ���������Լ�����ʽ�����ã��ѶȲ���


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��1.0L�����ܱ�������Ͷ��1mol CO2��2.75mol H2������Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����ʵ���ò�ͬ�¶ȼ�ѹǿ�£�ƽ��ʱ�״������ʵ����仯��ͼ��ʾ������˵����ȷ���ǣ�������
��1.0L�����ܱ�������Ͷ��1mol CO2��2.75mol H2������Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����ʵ���ò�ͬ�¶ȼ�ѹǿ�£�ƽ��ʱ�״������ʵ����仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | �÷�Ӧ������ӦΪ���ȷ�Ӧ | |
| B�� | ѹǿ��С��ϵΪp1��p2��p3 | |
| C�� | M���Ӧ��ƽ�ⳣ��K��ֵԼΪ1.04��10-2 | |
| D�� | ��p2��512 Kʱ��ͼ��N�� v��������v���棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼������Һ��ͨ�������̼��CO32-+CO2+H2O�T2HCO3- | |
| B�� | ����������Ũ���ᷴӦ��MnO2+4HCl��Ũ���TMn2++2Cl2��+2H2O | |
| C�� | ������������Һ�мӹ�������ʯ��ˮ��2HSO3-+Ca2++2OH-�TCaSO3��+2H2O+SO32- | |
| D�� | ������������ͭ��Һ��Ӧ��2Na+2H2O+Cu2+$\frac{\underline{\;\;��\;\;}}{\;}$2Na++Cu��OH��2��+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ݻ�Ϊ 1.0L ���ܱ������н��з�Ӧ��A��g��=B��g��+C��g����A �ij�ʼŨ��Ϊ 0.5mol?L-1�����¶�T1��T2 �£�A ��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺
���ݻ�Ϊ 1.0L ���ܱ������н��з�Ӧ��A��g��=B��g��+C��g����A �ij�ʼŨ��Ϊ 0.5mol?L-1�����¶�T1��T2 �£�A ��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

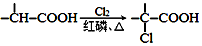

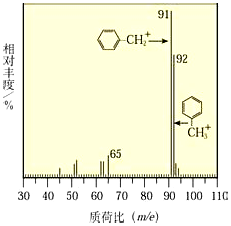
 +NaOH $��_{��}^{ˮ}$
+NaOH $��_{��}^{ˮ}$ +NaCl��
+NaCl�� ��
�� Ϊԭ����ȡ
Ϊԭ����ȡ  �ĺϳ�·��ͼ���ϳ�·��ͼʾ�����£�
�ĺϳ�·��ͼ���ϳ�·��ͼʾ�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na��O2 | B�� | Fe��FeCl3 | C�� | Fe��H2SO4 | D�� | AlCl3��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ����Һ | B�� | ��̪��Һ | C�� | ̼������Һ | D�� | �Ȼ�����Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com