
ЎҫМвДҝЎҝТТҙјКЗЦШТӘөДУР»ъ»Ҝ№ӨФӯБПЈ¬ҝЙУЙТТП©Л®әП·ЁЙъІъЈ¬·ҙУҰөД»ҜС§·ҪіМКҪИзПВЈәC2H4(g) + H2O(g) ![]() C2H5OH(g) Ј¬ПВНјОӘТТП©өДЖҪәвЧӘ»ҜВКУлОВ¶ИЈЁTЈ©ЎўС№ЗҝЈЁPЈ©өД№ШПө[ЖрКјn(C2H4) : n(H2O) =1:1]ЎЈ
C2H5OH(g) Ј¬ПВНјОӘТТП©өДЖҪәвЧӘ»ҜВКУлОВ¶ИЈЁTЈ©ЎўС№ЗҝЈЁPЈ©өД№ШПө[ЖрКјn(C2H4) : n(H2O) =1:1]ЎЈ

ПВБРУР№ШРрКцХэИ·өДКЗ
A. Y¶ФУҰөДТТҙјөДОпЦКөДБҝ·ЦКэОӘ![]()
B. XЎўYЎўZ¶ФУҰөД·ҙУҰЛЩВКЈәҰФ(X) >ҰФ(Y) >ҰФ(Z)
C. XЎўYЎўZ¶ФУҰөДЖҪәвіЈКэКэЦөЈәKX < KY <KZ
D. ФцҙуС№ЗҝЎўЙэёЯОВ¶ИҫщҝЙМбёЯТТП©өДЖҪәвЧӘ»ҜВК
Ўҫҙр°ёЎҝA
ЎҫҪвОцЎҝA. ҫЭНјҝЙЦӘЈ¬Yөг¶ФУҰТТП©өДЖҪәвЧӘ»ҜВКОӘ20%Ј¬ЖрКјn(C2H4) : n(H2O) =1:1Ј¬ЙиC2H4әНH2OөДЖрКјОпЦКөДБҝҫщОӘ1molЈ¬ёщҫЭИэ¶ОКҪ·ЁУРЈә
C2H4(g) + H2O(g) ![]() C2H5OH(g)
C2H5OH(g)
ЖрКјЈЁmolЈ© 1 1 0
ЧӘ»ҜЈЁmolЈ© 0.2 0.2 0.2
ЖҪәвЈЁmolЈ© 0.8 0.8 0.2
ФтЖҪәвКұТТҙјөДОпЦКөДБҝ·ЦКэОӘЈә ![]() =
=![]() Ј¬№КAХэИ·Ј»B. ТтёГ·ҙУҰКЗЖшМеМе»эјхРЎөДҝЙДж·ҙУҰЈ¬ЛщТФС№ЗҝФҪҙуЈ¬ТТП©өДЖҪәвЧӘ»ҜВКФҪҙуЈ¬ФтҪбәПНјПуҝЙөГЈәP1ЈјP2ЈјP3Ј¬ЗТXЎўYЎўZИэөг¶ФУҰөДОВ¶ИФҪАҙФҪёЯЈ¬ЛщТФXЎўYЎўZ¶ФУҰөД·ҙУҰЛЩВКЈәҰФ(X) ЈјҰФ(Y) ЈјҰФ(Z)Ј¬№КBҙнОуЈ»C. ҫЭНјҝЙЦӘЈ¬ЙэёЯОВ¶ИЈ¬ТТП©өДЖҪәвЧӘ»ҜВКҪөөНЈ¬ЛөГчёГ·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬ЙэёЯОВ¶ИЖҪәвДжПтТЖ¶ҜЈ¬ЖҪәвіЈКэјхРЎЈ¬ФтXЎўYЎўZ¶ФУҰөДЖҪәвіЈКэКэЦөЈәKX Јҫ KY ЈҫKZЈ¬№КCҙнОуЈ»D. ТтёГ·ҙУҰКЗЖшМеМе»эјхРЎөДҝЙДж·ҙУҰЈ¬ФтС№ЗҝФҪҙуЈ¬ТТП©өДЖҪәвЧӘ»ҜВКФҪҙуЈ¬УЦТтёГ·ҙУҰКЗ·ЕИИ·ҙУҰЈ¬ЙэёЯОВ¶ИЖҪәвДжПтТЖ¶ҜЈ¬ТТП©өДЖҪәвЧӘ»ҜВКҪөөНЈ¬№КDҙнОуЈ»ҙр°ёСЎAЎЈ
Ј¬№КAХэИ·Ј»B. ТтёГ·ҙУҰКЗЖшМеМе»эјхРЎөДҝЙДж·ҙУҰЈ¬ЛщТФС№ЗҝФҪҙуЈ¬ТТП©өДЖҪәвЧӘ»ҜВКФҪҙуЈ¬ФтҪбәПНјПуҝЙөГЈәP1ЈјP2ЈјP3Ј¬ЗТXЎўYЎўZИэөг¶ФУҰөДОВ¶ИФҪАҙФҪёЯЈ¬ЛщТФXЎўYЎўZ¶ФУҰөД·ҙУҰЛЩВКЈәҰФ(X) ЈјҰФ(Y) ЈјҰФ(Z)Ј¬№КBҙнОуЈ»C. ҫЭНјҝЙЦӘЈ¬ЙэёЯОВ¶ИЈ¬ТТП©өДЖҪәвЧӘ»ҜВКҪөөНЈ¬ЛөГчёГ·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬ЙэёЯОВ¶ИЖҪәвДжПтТЖ¶ҜЈ¬ЖҪәвіЈКэјхРЎЈ¬ФтXЎўYЎўZ¶ФУҰөДЖҪәвіЈКэКэЦөЈәKX Јҫ KY ЈҫKZЈ¬№КCҙнОуЈ»D. ТтёГ·ҙУҰКЗЖшМеМе»эјхРЎөДҝЙДж·ҙУҰЈ¬ФтС№ЗҝФҪҙуЈ¬ТТП©өДЖҪәвЧӘ»ҜВКФҪҙуЈ¬УЦТтёГ·ҙУҰКЗ·ЕИИ·ҙУҰЈ¬ЙэёЯОВ¶ИЖҪәвДжПтТЖ¶ҜЈ¬ТТП©өДЖҪәвЧӘ»ҜВКҪөөНЈ¬№КDҙнОуЈ»ҙр°ёСЎAЎЈ


 ГыРЈҝОМГПөБРҙр°ё
ГыРЈҝОМГПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁЦРХэИ·өДКЗ
A.ұкЧјЧҙҝцПВЈ¬1molЛ®өДМе»эКЗ22.4LB.1molИОәОЖшМеЈ¬Ме»эҫщОӘ22.4L
C.1molO2ФЪұкЧјЧҙҝцПВөДМе»эФјОӘ22.4LD.ұкЧјЧҙҝцПВЈ¬ЖшМеөДДҰ¶ыМе»эКЗ22.4L
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјЧ°ЦГЦЖИЎдеұҪЈ¬»ШҙрПВБРОКМвЈә

(1)РҙіцAЦР·ҙУҰөД»ҜС§·ҪіМКҪЈә_______________________Ј»
(2)CЦРКў·ЕCCl4өДЧчУГКЗ___________________________Ј»
(3)DЦРјУИлПхЛбТшИЬТәЈ¬КөСйәуИЬТәЦРДЬҝҙөҪөДКөСйПЦПуОӘ_____________________Ј»
(4)іЈУГУЪјшұрұҪәНјЧұҪөДКФјБОӘ_________________Ј»
(5)EОпЦК·ЦЧУКҪОӘC8H10Ј¬ЗТұҪ»·ЙПөДТ»ВИҙъОпЦ»УРТ»ЦЦЈ¬ФтEөДГыіЖОӘ_____________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТТНйЈЁC2H6Ј©ЧчОӘТ»ЦЦРВДЬФҙФЪ»ҜС§БмУтУҰУГ№г·әЈ¬Зл»ШҙрПВБРОКМвЈә(ИзНјЛщКҫЈ¬Ч°ЦГўсОӘТТНйИјБПөзіШ(өзҪвЦКИЬТәОӘKOHИЬТә)Ј¬НЁ№эЧ°ЦГўтКөПЦМъ°фЙП¶ЖНӯЎЈ
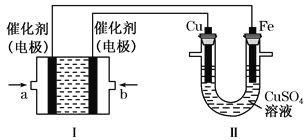
ўЩaҙҰУҰНЁИл______(МоЎ°C2H6Ўұ»тЎ°O2Ўұ)Ј¬aҙҰөзј«ЙП·ўЙъөДөзј«·ҙУҰКҪКЗ____________________________________Ј»
ўЪөз¶ЖҪбКшәуЈ¬Ч°ЦГўсЦРИЬТәөДpH______(МоРҙЎ°ұдҙуЎұЎ°ұдРЎЎұ»тЎ°І»ұдЎұЈ¬ПВН¬)Ј¬Ч°ЦГўтЦРCu2Ј«өДОпЦКөДБҝЕЁ¶И______Ј»
ўЫөз¶ЖҪбКшәуЈ¬Ч°ЦГўсИЬТәЦРөДТхАлЧУіэБЛOHЈӯТФНв»№ә¬УР___________(әцВФЛ®Ҫв)Ј»ФЪҙЛ№эіМЦРИфНкИ«·ҙУҰЈ¬Ч°ЦГўтЦРТхј«ЦКБҝұд»Ҝ12.8 gЈ¬ФтЧ°ЦГўсЦРАнВЫЙППыәДТТНй________L(ұкЧјЧҙҝцПВ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝT KКұЈ¬Пт2.0 LәгИЭГЬұХИЭЖчЦРідИл0.10 mol COCl2Ј¬·ўЙъ·ҙУҰCOCl2(g)![]() Cl2(g)Ј«CO(g)Ј¬ҫӯ№эТ»¶ОКұјдәу·ҙУҰҙпөҪЖҪәвЎЈ·ҙУҰ№эіМЦРІвөГөДІҝ·ЦКэҫЭјыПВұнЈә
Cl2(g)Ј«CO(g)Ј¬ҫӯ№эТ»¶ОКұјдәу·ҙУҰҙпөҪЖҪәвЎЈ·ҙУҰ№эіМЦРІвөГөДІҝ·ЦКэҫЭјыПВұнЈә
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2)/mol | 0 | 0.030 | 0.039 | 0.040 | 0.040 |
ПВБРЛө·ЁХэИ·өДКЗ( )
A. ұЈіЦЖдЛыМхјюІ»ұдЈ¬ЙэёЯОВ¶ИЈ¬ЖҪәвКұc(Cl2)ЈҪ0.038 molЎӨLЈӯ1Ј¬Фт·ҙУҰөДҰӨHЈј0
B. ·ҙУҰФЪЗ°2 sөДЖҪҫщЛЩВКv(CO)ЈҪ0.015 molЎӨLЈӯ1ЎӨsЈӯ1
C. ұЈіЦЖдЛыМхјюІ»ұдЈ¬ЖрКјКұПтИЭЖчЦРідИл0.12 mol COCl2Ўў0.06 mol Cl2әН0.06 mol COЈ¬·ҙУҰҙпөҪЖҪәвЗ°өДЛЩВКЈәvХэЈјvДж
D. ұЈіЦЖдЛыМхјюІ»ұдЈ¬ЖрКјКұПтИЭЖчЦРідИл0.10 mol Cl2әН0.08 mol COЈ¬ҙпөҪЖҪәвКұЈ¬Cl2өДЧӘ»ҜВКҙуУЪ60%
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРёчЧйОпЦК°ҙЛбЎўјоЎўСО·ЦАаЛіҙОЕЕБРЈ®ХэИ·өДКЗЈЁ Ј©
A.БтЛбЎўҙҝјоЎўМјЛбёЖ
B.ПхЛбЎўЙХјоЎўКіСО
C.ұщҙЧЛбЎўҙҝјоЎўҙЧЛбДЖ
D.СОЛбЎўКмКҜ»ТЎўҝБРФДЖ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ·ЦЧУКҪОӘC7H16ЎўC5H11ClЎўC5H10ЈЁБҙЧҙЈ¬І»ҝјВЗҝХјд№№РНЈ©өДН¬·ЦТм№№МеөДКэДҝ·ЦұрУРЈЁ Ј©ЦЦ
A. 9,8,5 B. 8,9,5 C. 9,9,6 D. 8,8,6
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁХэИ·өДКЗ
A.ВИЖшДЬҪ«өҘЦКМъ»№ФӯОӘВИ»ҜМъ
B.СОЛбјИУРСх»ҜРФУЦУР»№ФӯРФ
C.ЗвЖшФЪВИЖшЦРҫзБТИјЙХЈ¬»рСжіКІФ°ЧЙ«Ј¬УР°ЧСМЙъіЙ
D.ОӘІв¶ЁРВЦЖВИЛ®өДpHЈ¬УГІЈБ§°фХәИЎТәМеөОФЪpHКФЦҪЙПЈ¬УлұкЧјұИЙ«ҝЁ¶ФХХјҙҝЙ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДі№Өі§·ПЛ®ЦРә¬УОАлМ¬ВИЈ¬НЁ№эПВБРКөСйІв¶ЁЖдЕЁ¶ИЎЈ
ўЩИЎЛ®Сщ10Ј®0mlУЪЧ¶РОЖҝЦРЈ¬јУИл10Ј®0mlөДKIИЬТә(ЧгБҝ)Ј¬·ўЙъөД·ҙУҰОӘЈәCl2+2KIЈҪ2KCl+I2Ј¬өОИлЦёКҫјБ2~3өОЎЈ
ўЪўЪИЎТ»өО¶Ё№ЬТАҙОУГЧФАҙЛ®ЎўХфБуЛ®Пҙҫ»әуЈ¬ФЩУГ0.01molЎӨL-1Na2S2O3ИЬТәИуПҙЈ¬И»әуЧ°Ил0.01molЎӨL-1Na2S2O3ИЬТәөҪ0ҝМ¶ИТФЙПЈ¬ЕЕіцПВ¶ЛјвЧмДЪөДЖшЕЭЈ¬өчХыТәГжЦБ0ҝМ¶И»т0ҝМ¶ИПВДіТ»О»ЦГЈ¬јЗПВ¶БКэЎЈ
ўЫҪ«Ч¶РОЖҝЦГУЪөО¶Ё№ЬПВҪшРРөО¶ЁЈ¬·ўЙъөД·ҙУҰОӘЈәI2+2Na2S2O3=2NaI+ 2Na2S4O6 КФ»ШҙрПВБРОКҙрЈә
ЈЁ1Ј©ІҪЦиўЩјУИлөДЦёКҫјБКЗ_______________________________ЎЈ
ЈЁ2Ј©ІҪЦиўЪУҰК№УГ________КҪөО¶Ё№ЬЎЈ
ЈЁ3Ј©ЕР¶ПҙпөҪөО¶ЁЦХөгөДКөСйПЦПуКЗ___________________________________Ј»
ЈЁ4Ј©УГ0.1032mol/L HClИЬТәөО¶ЁОҙЦӘЕЁ¶ИөДNaOHИЬТәЈ¬ПВБРЗйҝц¶ФКөСйҪб№ыОЮУ°ПмөДКЗ____________
A.ЛбКҪөО¶Ё№ЬОҙУГұкЧјСОЛбИЬТәИуПҙ
B.Ч¶РОЖҝОҙУГҙэІвТәИуПҙ
C.өО¶ЁЗ°өО¶Ё№ЬјвЧмЦРУРТ»ЖшЕЭЈ¬өО¶ЁәуЖшЕЭПыК§БЛ
D.өО¶ЁКұҪ«ұкЧјТәҪҰіцЧ¶РОЖҝНв
ЈЁ5Ј©МјЛбH2CO3Ј¬K1=4.3ЎБ10-7Ј¬K2=5.6ЎБ10-11,ІЭЛбH2C2O4Ј¬K1=5.9ЎБ10-2Ј¬K2=6.4ЎБ10-50.1 mol/L Na2CO3ИЬТәөДpH____________0.1 mol/L Na2C2O4ИЬТәөДpHЎЈ(СЎМоЎ°ҙуУЪЎұЎўЎ°РЎУЪЎұ»тЎ°өИУЪЎұ)ЎЈИфҪ«өИЕЁ¶ИөДІЭЛбИЬТәәНМјЛбИЬТәөИМе»э»мәПЈ¬ИЬТәЦРёчЦЦАлЧУЕЁ¶ИҙуРЎөДЛіРтХэИ·өДКЗ_____________ЎЈ(СЎМоұаәЕ)
AЈ®c(H+)Јҫc(HC2O4-)Јҫc[HCO3-)Јҫc[CO32-) BЈ®c(HCO3-)Јҫc(HC2O4-)Јҫc(C2O42-)Јҫc(CO32-)
CЈ®c(H+)Јҫc(HC2O4-)Јҫc(C2O42-)Јҫc(CO32-) DЈ®c(H2CO3) Јҫc(HCO3-)Јҫc(HC2O4-)Јҫc(CO32-)
ЈЁ6Ј©ТСЦӘЈәўЩДСИЬөзҪвЦКөДИЬ¶И»эіЈКэЈәKspЈЁCaF2Ј©ЈҪ1.5ЎБ10Јӯ10 ўЪ25ЎжКұЈ¬2.0ЎБ10Јӯ3molЎӨL-1Зв·ъЛбЛ®ИЬТәЦРЈ¬өчҪЪИЬТәpHЈЁәцВФМе»эұд»ҜЈ©Ј¬өГөҪcЈЁHFЈ©ЎўcЈЁF-Ј©УлИЬТәpHөДұд»Ҝ№ШПөЈ¬ИзПВНјЛщКҫЈәЗлёщҫЭТФПВРЕПў»ШҙрПВБРОКМвЈә
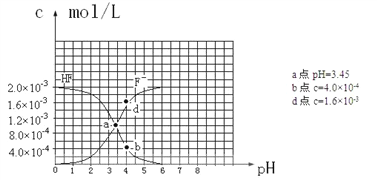
ўЩ25ЎжКұЈ¬HFөзАлЖҪәвіЈКэөДКэЦөKaЎЦ_______________________________ЎЈ
ўЪ4.0ЎБ10Јӯ3 molЎӨL-1HFИЬТәУл4.0ЎБ10Јӯ4 molЎӨL-1 CaCl2ИЬТәөИМе»э»мәПЈ¬өчҪЪ»мәПТәpHОӘ4.0ЈЁәцВФөчҪЪ»мәПТәМе»эөДұд»ҜЈ©Ј¬НЁ№эБРКҪјЖЛгЛөГчКЗ·сУРіБөнІъЙъЎЈ_______________________________________
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com