
����Ŀ���ϳɰ�����H2ȡ��CH4��CH4��O2���ó�CO2��H2����Ӧ�٣���Ȼ��CH4��O2��Ӧ��������CO2��H2O����Ӧ�ڣ�������ˮ����ʱ��H2O��CH4��Ӧ����Ӧ�ۣ����±� Ϊ������Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ��K��

��1����Ӧ�ٵ�ƽ�ⳣ��K�ٵı���ʽΪ_______________��
��2����Ӧ�٢ڢ۵�ƽ�ⳣ��K�١�K�ڡ�K��֮��Ĺ�ϵΪK��=_____________���ú�K�١� K�۵�ʽ�ӱ�ʾ������Ӧ�٢ڢ۵ķ�Ӧ�ʱ䣺��H�١���H�ڡ���H��֮��Ĺ�ϵΪ��H��= _____________���ú���H�ڡ���H�۵�ʽ�ӱ�ʾ����
��3�����������£���Ӧ�۵������뷴Ӧ���̹�ϵӦ��Ӧ��ͼ�е�_____________����Ӧ�� �������뷴Ӧ���̹�ϵӦ��Ӧ��ͼ�е�_____________��

��4��Ϊʹ��Ӧ�����ܰ�����H2�ķ�����У���ֻ���Ƿ�Ӧ�ۣ��Ҳ����ͷ�Ӧ���ʣ��ɲ� ȡ__________��ʩ����ֻ���Ƿ�Ӧ�٢ڣ�����ȡ���´�ʩ�⣬���ɲ�ȡ_____________��д��������ʩ���ɣ���
��5��250��ʱ�������Ͻ�Ϊ����������CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)����40L ���ܱ�������ͨ��6molCO2(g)��6molCH4(g)��ƽ��ʱ�����ϵ��CH4��������� Ϊ10%������������ܶ�Ϊ______g/L��CO2��ת����Ϊ__________��������λ��Ч���֣���
2CO(g)+2H2(g)����40L ���ܱ�������ͨ��6molCO2(g)��6molCH4(g)��ƽ��ʱ�����ϵ��CH4��������� Ϊ10%������������ܶ�Ϊ______g/L��CO2��ת����Ϊ__________��������λ��Ч���֣���
���𰸡�![]() K��2/K�� (��H������H��)/2 D B �����¶� CH4��O2Ͷ���Ϊ1��1����ʹ��ֻ����Ӧ�ٵĴ����������ʵ���ѹ 9 66.7%
K��2/K�� (��H������H��)/2 D B �����¶� CH4��O2Ͷ���Ϊ1��1����ʹ��ֻ����Ӧ�ٵĴ����������ʵ���ѹ 9 66.7%
��������
��1�����ݻ�ѧƽ�ⳣ������ʽ��K��=![]() ��
��
��2��K��=![]() ��K��=
��K��=![]() ��K��=
��K��=![]() �����K��=K��2/K��������Ŀ�귴Ӧ����ʽ����H��=(��H������H��)/2��
�����K��=K��2/K��������Ŀ�귴Ӧ����ʽ����H��=(��H������H��)/2��
��3�����ݱ������ݣ������¶ȵ����ߣ���Ӧ�۵Ļ�ѧƽ�ⳣ����������������ԭ������Ӧ�۵�����Ӧ����Ϊ���ȷ�Ӧ������H>0����Ӧ����������������������������ͼD��ȷ��ͬ����Ӧ������ӦΪ���ȷ�Ӧ����Ӧ����������������������������Ӧ��ƽ�ⳣ����˵����ܽϵͣ���ͼB��ȷ��
��4������(3)����Ӧ��Ϊ���ȷ�Ӧ����Ӧ������Ӧ�����ƶ������������¶ȣ���Ӧ�٢�������Ӧ�����ƶ��������ͷ�Ӧ���ʣ����Բ�ȡ�Ĵ�ʩΪCH4��O2Ͷ���Ϊ1��1����ʹ��ֻ����Ӧ�ٵĴ����������ʵ���ѹ��
��5����ﵽƽ������CO2�����ʵ���Ϊxmol��CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
6 6 0 0
x x 2x 2x
6��x 6��x 2x 2x
CH4���������(6��x)/(12��2x)��100%=10%�����x=4����ֶ������壬����������Ϊ(6mol��44g��mol��1��6mol��14g��mol��1)=360g���������Ϊ40L���������ܶ�Ϊ360g/40L=9g��L��1��CO2��ת����Ϊ4mol/6mol��100%=66.7%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ڣ�100 ��ĵ����ºϳ���һ����X��������ͺ˴Ź������ױ���������е���ԭ�������Ļ�ѧ����û�����𣬸��ݷ����������˸÷��ӵ����ģ����ͼ��ʾ������˵���в���ȷ����(����)
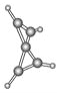
A. �÷��ӵķ���ʽΪC5H4
B. �÷�����̼ԭ�ӵĻ�ѧ������2��
C. �÷����е���ԭ�ӷֲ����������ֱ��ƽ����
D. �÷�����ֻ��C��C����û��![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�ѧ��Ӧ�У������ѵĹ��ۼ��У��������Ѧļ����� �� ��
A. N2��3H2  2NH3
2NH3
B. 2C2H2��5O2![]() 2H2O��4CO2
2H2O��4CO2
C. Cl2��H2![]() 2HCl
2HCl
D. C2H4��H2![]() C2H6
C2H6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ��������ʻ�����������ص���
A. �����������ܶ���373 KʱΪ1.335 g/L����297 KʱΪ2.5 g/L
B. ���ǻ������ᣨ �����۵�Ϊ159�棬���ǻ������ᣨ
�����۵�Ϊ159�棬���ǻ������ᣨ![]() �����۵�Ϊ213��
�����۵�Ϊ213��
C. ��������ˮ�����Ҵ�����ˮ������Ȼ���
D. HF�ֽ�ʱ���յ�������HCl�ֽ�ʱ���յ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�Լ�Ӧ���������ʺ���̬������Ч���Ʊ��棺
(1)�����Լ�Ӧ������____________�У�Һ���Լ�������____________�У������ֽ���Լ�(�磺ŨHNO3��AgNO3��)Ӧ��____________ɫ�Լ�ƿ���档�����(HF)��Ͳ����е�SiO2ǿ�ҷ�Ӧ����ʴ������Ӧ��____________��ţ������ơ���Ӧ������____________�У���������Ӧ�ñ�����____________�С�
(2)������ˮ�豣������ɫ�Լ�ƿ�У�ԭ����__________________��
(3)ʵ���������Ƶ�����������Һ��һ��Ҫ��������___________����ֹ�ڿ����б��ʡ�
(4)��ʢ��Ũ������Լ�ƿ��ǩ��ӡ�����о�ʾ��ǣ�˵��Ũ�������_______�ԡ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʱ����0.1mol/L��һԪ����ĵ����Ϊ1%��������˵����ȷ���ǣ� ��
A.����Һ��pH=11
B.����Һ��pH=3
C.��������0.1mol/LHCl��������Һ��pH=7
D.��������pH=3�������������Һ��pH=7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ʳ������Ա仯�ľ��������ǣ� ��
A. Ԫ��ԭ�Ӱ뾶��С�������Ա仯
B. Ԫ�����ԭ���������ε���
C. Ԫ��ԭ�����������Ų��������Ա仯
D. Ԫ�ص���������ϼ۳������Ա仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵȼ��ú��ʯ�͵Ȼ�ʯȼ���ͷų�������������(NOx)��CO2��CO��SO2�����壬������Ⱦ�������Է���������������̼����������ʵ����ɫ�������������á�
I.��������֪��H2����ֵΪ142.9 kJ/g(��ֵ�DZ�ʾ��λ������ȼ����ȫȼ��ʱ���ų�������)��
N2(g) + 2O2(g) = 2NO2(g) ��H= +133 kJ/mol
H2O(g) =H2O(l) ��H=- 44 kJ/mol
���������£�H2��ԭNO2����ˮ������N2���Ȼ�ѧ����ʽΪ_____
��.��̼��
(1)��2L�����ܱ������м���2 mol CO2��6 mol H2�����ʵ��Ĵ��������£�������Ӧ:
CO2(g)+3H2(g)CH3OH(l)+H2O(l)������������˵���˷�Ӧ�ﵽƽ��״̬����________��
A����������ƽ��Ħ���������ֲ���B��CO2��H2������������ֲ���
C��CO2��H2��ת������� D�����������ܶȱ��ֲ���
E.1 mol CO2���ɵ�ͬʱ��3 mol H��H������
(2)�ı��¶ȣ�ʹ��ӦCO2(g) + 3H2(g)CH3OH(g) + H2O(g)��H<0�е��������ʶ�Ϊ��̬,��ʼ�¶������ͬ(T1�桢2L�ܱ�����)����Ӧ�����в������ݼ��±���
���º��� | ��Ӧʱ�� | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
��ӦI | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
��ӦII | 0 min | 0 | 0 | 2 | 2 |
�ٴﵽƽ��ʱ����ӦI��II�Աȣ�ƽ��ʱCH3OH��Ũ��c(I)___________c(II)��(����>����<������=������ͬ)������ӦI��������Ϊ���Ⱥ��ݣ�ƽ��ʱ��ƽ�ⳣ���뷴ӦI�ıȽ�_________(��������������С������������)
�ڶԷ�Ӧ��ǰ10min�ڵ�ƽ����Ӧ����v(CH3OH)=________ ,���������������£����¶ȸ�ΪT2,���30minʱ��H2�����ʵ���Ϊ3.2mol,��T1____T2(����>����<������=��)��30minʱֻ���������ٳ���1molCO2(g)��1molH2O(g),��ƽ��_______�ƶ�(����������������������������)
(3)����ȼ�ϵ�ؿ����������������ʡ���ͼ�����ü���ȼ�ϵ�ص��100mL 1mol��L -1ʳ��ˮ,���һ��ʱ���,�ռ�����״���µ�����2.24L(�������Һ�������)��

�ټ���ȼ�ϵ�صĸ�����Ӧʽ: ____________________________________
�ڵ�����Һ��pH= __________________________(��������������������Һ��Ӧ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NH4)2Cr2O7�������л��ϳɴ�����ýȾ������ӰҺ�ȡ�ij��ѧ��ȤС���(NH4 )2Cr2O7�IJ������ʼ���ɽ���̽����
��֪��Cr2O72-(��ɫ��+ H2O 2CrO42-����ɫ��+2H+����ش��������⣺
�����Թ��м�������(NH4)2Cr2O7���壬�μ�����ŨK0H��Һ�����ȣ��۲쵽����Ҫ������________��
��Ϊ̽��(NH4)2Cr2O7 (Ħ������Ϊ252 g/mol)�ķֽ�������ͼ���Ӻ�װ�ã���A�м���5.040 g��Ʒ����ʵ�顣
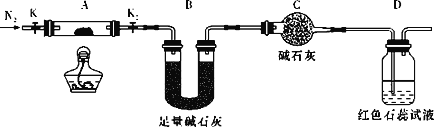
������C��������______________��
�����Ӻ�װ�ã���ȼ�ƾ���֮ǰ������еı�Ҫ������_________________________��
�۷�Ӧ��������ȻҪͨһ��ʱ��ĵ�����ԭ����_______________________��
�ܼ���A�����أ��۲쵽D����Һ����ɫ��ͬʱ���A�в�����ΪCr2O3��B�������ı仯Ϊ1.44 g��д���ظ���識��ȷֽⷴӦ�Ļ�ѧ����ʽ:_________��
(3)ʵ���ҳ��ü�ȩ���ⶨ��(NH4)2Cr2O7����Ʒ�е����������������ʲ�������Ӧ�����䷴Ӧԭ��Ϊ 2Ba2++Cr2O72- + H2O = 2BaCrO 4��+2H+��4NH4++6HCHO = 3H++6H2O+(CH2)6N4H+ [�ζ�ʱ��1 mo1 (CH2)6N4H+ �� 1 mo1 H+ �൱]��Ȼ���� NaOH ����Һ�ζ���Ӧ���ɵ��ᡣ
ʵ�鲽�裺��ȡ��Ʒ5.600 g�����500 mL��Һ����ȡ25.00 mL��Ʒ��Һ�� 250 mL��ƿ�У����Ȼ�����ҺʹCr2O72-��ȫ��������10 mL 20.00 mol��L��1�����Լ�ȩ��Һ��ҡ�ȡ�����5 min����12�η�̪��Һ����0.200 mo1 L-1 NaOH ����Һ�ζ����յ㡣�ظ���������3�Σ����յζ���ȥNa0H����Һ�����ƽ��ֵΪ20.00 mL��
�����ζ��յ�ʱ�����Ӷ�������ⶨ���__________(�ƫ�� ��ƫС������Ӱ�족����
�ڵζ�����ø���Ʒ�е�����������Ϊ_________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com