
| △c |
| △t |
| △c |
| △t |
| 0.32mol/L |
| 8min |


科目:高中化学 来源: 题型:
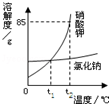
| A、硝酸钾的溶解度随温度升高而减小 |
| B、t2℃时,100g饱和硝酸钾溶液中溶有硝酸钾85g |
| C、t1℃时,氯化钠和硝酸钾的溶解度相同 |
| D、将t1℃时的硝酸钾饱和溶液升温到t2℃,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.查看答案和解析>>
科目:高中化学 来源: 题型:
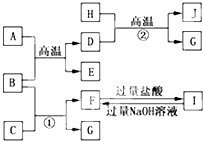 如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属,G是气体,J是磁性材料,常温下H为无色液体.
如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属,G是气体,J是磁性材料,常温下H为无色液体.查看答案和解析>>
科目:高中化学 来源: 题型:
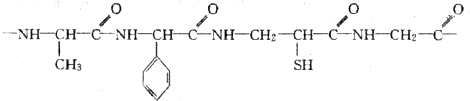
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,回答:
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,回答:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、Ca2+、Na+、NO
| ||||
B、K+、Ba2+、Cl-、NO
| ||||
C、HCO
| ||||
D、Ca2+、Cl-、K+、NO
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com