


科目:高中化学 来源:2011-2012年江苏省无锡市高一下学期期中考试化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.原子及其离子的核外电子层数等于该元素所在周期数
B.稀有气体元素原子的最外层电子数都是8
C.元素周期表从ⅢB到ⅡB 10个纵行的元素都是金属元素
D.短周期元素中,若两种元素的原子序数相差8,则它们的周期数一定相差1
查看答案和解析>>
科目:高中化学 来源:2013届浙江省嘉兴八校高二下学期期中联考化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.在稀溶液中1mol酸和1mol碱完全反应所放出的热量,叫做中和热
B.在101kPa时1mol物质燃烧时的反应热叫做该物质的标准燃烧热
C.热化学方程式中,各物质前的化学计量数不表示分子个数
D.如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应
查看答案和解析>>
科目:高中化学 来源:2014届浙江东阳中学、兰溪一中高一下学期期中考试化学卷(解析版) 题型:选择题
如下图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,则下列叙述中正确的是( )
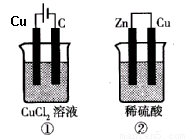
A.产生气体的体积:①>②
B.溶液的pH变化:①不变 ②增大
C.①和②中铜电极均失电子
D.电极反应式:①中阳极 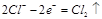 ②中负极
②中负极 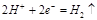
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.在101kPa时1mol物质燃烧时的反应热叫做该物质的标准燃烧热
B.热化学方程式中,各物质前的化学计量数不表示分子个数
C.如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应。
D.化学反应的自发性仅由反应的焓变或熵变决定
查看答案和解析>>
科目:高中化学 来源:2010-2011学年陕西省高三上学期摸底考试化学试卷 题型:选择题
设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,11.2L氧气所含的原子数为NA
B.1.7g的NH+4离子中含有的电子数为NA
C.常温常压下,48gO3含有的氧原子数为3NA
D.2.4g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com