
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
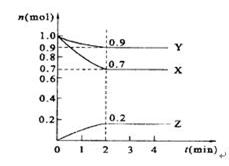
(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程为 ;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)= ,
(4)当反应进行到第 min,该反应达到平衡。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列五种短周期元素的某些性质如表所示(其中只有W,Y、Z为同周期元素)。
| 元素代号 | X | W | Y | Z | Q |
| 原子半径(×10-12 m) | 37 | 64 | 66 | 70 | 154 |
| 主要化合价 | +1 | -1 | -2 | +5、-3 | +1 |
下列说法正确的是( )
A.由Q与Y形成的化合物中只存在离子键
B.Z与X之间形成的化合物具有还原性
C.由X、Y、Z三种元素形成的化合物,其晶体一定是分子晶体
D.Y与W形成的化合物,Y显负价
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F是周期表中短周期的六种元素,有关性质或结构信息如下表:
| 元素 | 有关性质或结构信息 |
| A | 雷雨天大气中会有A的一种单质生成 |
| B | B离子与A离子电子数相同,且是所在周期中单核离子半径最小的 |
| C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
| D | D是制造黑火药的一种成分,也可用于杀菌消毒 |
| E | E与D同周期,且在该周期中原子半径最小 |
| F | F的简单氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
(1)A与C以原子个数比为1:1形成的化合物的电子式为_______,将0.6 mol该化合物投入到100 mL 3 mol/L BE3溶液中的离子方程式为________________、________________。
(2)F的简单氢化物是由________________(填“极性”或“非极性”)键形成的________________(填“极性”或“非极性”)分子,写出实验室制备该氢化物的化学方程式:________________。
(3)如图实验可用于证明D、E的非金属性的强弱。
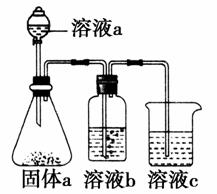
①溶液a和b分别为________________、________________(写化学式)。
②溶液a与固体a反应的离子方程式为________________。
③非金属性D________________E(填“>”或“<”),请从原子结构的角度解释原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某主族元素R的最高正化合价与负化合价代数和为6,下列叙述正确的是:( )
A.R一定是第VIIA族元素 B.R的最高价氧化物为RO3
C.R的气态氢化物能燃烧 D.R的气态氢化物易溶于水显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又属于吸热反应的是
A.铝片与稀盐酸反应 B.甲烷在氧气中燃烧
C.灼热的炭与二氧化碳反应 D.Ba(OH)2·8H2O与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定量的密闭容器中进行反应:N2(g)+3H2 2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L。当反应达到平衡时,可能存在的数据是
2NH3(g)。已知反应过程中某一时刻N2、H2、NH3的浓度分别为0.1 mol/L、0.3 mol/L、0.2 mol/L。当反应达到平衡时,可能存在的数据是
A.N2为0.2 mol/L,H2为0.6 mol/L B.N2为0.15 mol/L
C.N2、H2均为0.18 mol/L D.NH3为0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。实验所用仪器如下:

(1)写出发生装置中进行反应的化学方程式: ;
(2)上述仪器的连接顺序是(填接口字母):E接 , 接 , 接 , 接 。
(3)实验前,应该进行的一项操作是 。
(4)饱和食盐水的作用是 。
(5)若实验中得到标况下11.2L氯气,被氧化的HCl的物质的量为 ,此时转移的电子数是 。
(6)下列试剂中,可以用来吸收残余氯气的是 。
A.饱和食盐水 B.氢氧化钠溶液 C.碳酸钠溶液 D.浓硫酸
(7)工业上制取氯气的离子方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com