
| A. | 甲和丙的K相同 | B. | 乙和丙的正反应速率相同 | ||
| C. | 乙中SO3的体积分数小于丙 | D. | 转化率:α甲(SO2)+α乙(SO3)<1 |
分析 A、甲是绝热恒容,反应放热反应,所以甲容器中温度升高,平衡常数随温度变化;
B、乙容器恒温恒容,充入2molSO3,丙容器恒温恒压,充入2molSO3,随反应进行气体体积增大,压强增大,丙中体积增大为了维持恒压,乙中反应速率大;
C、乙容器恒温恒容,充入2molSO3,丙容器恒温恒压,充入2molSO3,随反应进行气体体积增大,压强增大,丙中体积增大为了维持恒压,乙中反应速率大,丙中平衡逆向进行,三氧化硫体积分数减小;
D、若甲容器恒温恒容,充入2molSO2和1molO2,乙容器恒温恒容,充入2molSO3,达到相同的平衡状态,转化率:α甲(SO2)+α乙(SO3)=1,但甲容器是绝热容器,反应是放热反应,温度升高平衡逆向进行,则甲中二氧化硫转化率减小;
解答 解:A、甲是绝热恒容,反应放热反应,所以甲容器中温度升高,平衡常数随温度变化,平衡常数不同,故A错误;
B、乙容器恒温恒容,充入2molSO3,丙容器恒温恒压,充入2molSO3,随反应进行气体体积增大,压强增大,丙中体积增大为了维持恒压,速率减小,则乙中反应速率大,故B错误;
C、乙容器恒温恒容,充入2molSO3,丙容器恒温恒压,充入2molSO3,随反应进行气体体积增大,压强增大,丙中体积增大为了维持恒压,乙中反应速率大,丙中平衡逆向进行,三氧化硫体积分数减小,乙中SO3的体积分数大于丙,故C错误;
D、若甲容器恒温恒容,充入2molSO2和1molO2,乙容器恒温恒容,充入2molSO3,达到相同的平衡状态,转化率:α甲(SO2)+α乙(SO3)=1,但甲容器是绝热容器,反应是放热反应,温度升高平衡逆向进行,则甲中二氧化硫转化率减小,α甲(SO2)+α乙(SO3)<1,故D正确;
故选D.
点评 本题考查了化学平衡建立的过程分析判断,平衡影响因素的分析应用,注意容器和温度压强的特征理解,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 金刚石和石墨均为碳元素组成的单质 | |
| B. | CO2:弱电解质 | |
| C. | 蓝矾(CuSO4•5H2O)和干冰属于化合物,铁矿石属于混合物 | |
| D. | 醋酸:一元弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 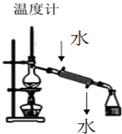 装置用于分离两种沸点相差较大的液体互溶混合物 | |
| B. | 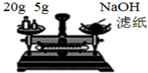 装置称量氢氧化钠固体 | |
| C. | 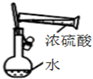 装置配制一定物质的量浓度的稀硫酸 | |
| D. |  装置检查容量瓶是否漏水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 小苏打溶液与乙酸溶液混合 HCO${\;}_{3}^{-}$+CH3COOH═CH3COO-+H2O+CO2↑ | |
| B. | 冷的氢氧化钠溶液中通入氯气:Cl2+2OH-═ClO-+Cl-+H2O | |
| C. | Fe2O3溶于HI溶液中 Fe2O3+6H++2I-═2Fe2++3H2O+I2 | |
| D. | 过量CO2通入NaAlO2溶液中:2AlO${\;}_{2}^{-}$+CO2+3H2O═2Al(OH)3↓+CO2${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 正 极 | 负 极 | 电解质溶液 | |
| A | Cu | Fe | FeCl3 |
| B | C | Fe | Fe(NO3)3 |
| C | Fe | Zn | Fe2(SO4)3 |
| D | Ag | Fe | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com