
(10分)(1)写出下列工业生产过程所涉及的主要化学方程式:
① 用铝热法炼铁____________________________________________________
② 电解法冶炼铝______________________________________________________
③ 湿法炼铜______________________________________________________
(2)海水中含有氯化镁,是镁的重要来源之一。从海水中制取镁,某同学设计了如下步骤:
①把贝壳制成石灰乳
②直接往海水中加石灰乳,沉降、过滤、洗涤沉淀物
③将沉淀物与盐酸反应,结晶、过滤、干燥产物
④将得到的产物熔融后电解。
下列说法不正确的是__________________(填代号)
A.此法的优点之一是原料来源丰富
B.进行①②③步骤的目的是从海水中提取氯化镁
C.第④步电解制镁是由于镁是很活泼的金属
D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应
步骤②不够合理,理由是
。
科目:高中化学 来源: 题型:阅读理解
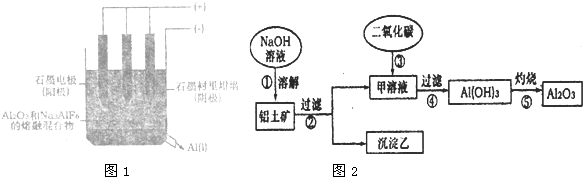
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| CO2 | CH4 | N2 | |
| 极化率 | 2.87 | 3.00 | 1.93 |
| 沸点 | -78.5 | -161 | -195.8 |



| MgCl2?6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
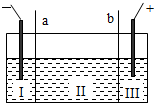 则以下叙述正确的是
则以下叙述正确的是查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下(不需添加另外的反应物),经不同的化学反应,可实现如下图的各种变化。其中,反应①、②属于非氧化还原反应。正盐A分解得到三种气体。X、F和Y为单质,其余为化合物。在高科技领域中常用液态F制造低温环境。Y常用来制取漂白粉。
请填空:

(1)写出下列物质的化学式:
A F X 。
(2)反应⑤的阴极产物为 。
(3)写出实际工业生产中X+F→D具体的反应条件 。
(4)当B过量时,写出B与W反应的离子方程式 。
(5)当D过量时,写出D与Y的反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com