
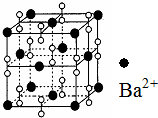
 钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,有关说法正确的是( )
钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如图所示,有关说法正确的是( )| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该氧化物的电子式为 | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有6个 |
分析 A.由阴阳离子构成的晶体为离子晶体,离子晶体中可能含有共价键;
B.该晶胞中Ba离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,过氧根离子个数=1+12×$\frac{1}{4}$=4,则钡离子和过氧根离子个数之比为4:4=1:1,据此确定化学式;
C.由B选项知晶体的化学式为Ba2O2,由图知两个氧原子以过氧根离子存在;
D.与每个Ba2+距离相等且最近的Ba2+个数=3×8×$\frac{1}{2}$.
解答 解:A.该晶胞是由金属阳离子钡离子和阴离子过氧根离子构成的,为离子晶体,故A错误;
B.该晶胞中Ba离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,过氧根离子个数=1+12×$\frac{1}{4}$=4,则钡离子和过氧根离子个数之比为4:4=1:1,其化学式为BaO2,故B错误;
C.由B选项知晶体的化学式为Ba2O2,由图知两个氧原子以过氧根离子存在,故该氧化物的电子式为 ,故C正确;
,故C正确;
D.与每个Ba2+距离相等且最近的Ba2+个数=3×8×$\frac{1}{2}$=12,故D错误;
故选:C.
点评 本题考查晶胞计算,侧重考查分析、计算、空间想象能力,以教材中氯化钠、氯化铯为例采用知识迁移方法解答离子晶体晶胞有关计算,难点是配位数的计算方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
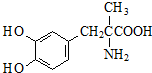
| A. | 分子式为C10H14NO4 | |
| B. | 分子中有一个手性碳原子 | |
| C. | 甲基多巴具有两性,且能发生酯化反应 | |
| D. | 1mol甲基多巴分子最多能与2 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

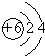 ;元素②的最高价氧化物结构式为:O=C=0;
;元素②的最高价氧化物结构式为:O=C=0;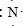 →
→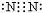 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.21的己烷所含的分子数为0.5 NA | |
| B. | 28g乙烯所含共用电子对数目为4 NA | |
| C. | 1mol苯乙烯中含有的C=C数为4NA | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2SO4•2Cr2(SO4)3 | B. | 2K2SO4•Cr2(SO4)3 | C. | K2SO4•Cr2(SO4)3 | D. | K2SO4•$\frac{1}{2}$Cr2(SO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | FeCl3溶液 | B. | 溴水 | ||
| C. | 酸性高锰酸钾溶液 | D. | NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com