
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且30分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中的溶液从色变为色时,停止滴定.
(2)滴定时边滴边摇动锥形瓶,眼睛应观察;
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 , 由此造成的测定结果(填偏高、偏低或无影响);
(4)步骤②缺少的操作是;
(5)如图,是某次滴定时的滴定管中的液面,其读数为mL;
(6)根据如表数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度为mol/L.
【答案】
(1)红;无
(2)B
(3)待测溶液润洗锥形瓶;偏高
(4)用标准液润洗滴定管
(5)22.60
(6)0.08
【解析】解:(1)标准酸滴定NaOH溶液,以酚酞作指示剂,滴定终点时,溶液的颜色由红色变为无色,并且30S内不变色;所以答案是:红;无;(2)滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶中颜色变化,以判定终点;所以答案是:B;(3)根据待测溶液润洗锥形瓶,会使的待测液的物质的量增多,造成V(标准)偏大,根据根据c(待测)= ![]() 分析,可知c(待测)偏大;所以答案是:待测溶液润洗锥形瓶;偏高;(4)根据酸式滴定管用蒸馏水洗净后,应用标准盐酸润洗,以防被稀释;所以答案是:用标准液润洗滴定管;(5)待测液的物质的量不变,读数时目光平视,凹液面最低点与刻度线相切,所以读数为22.60mL;所以答案是:22.60;(6)两次消耗的盐酸标准液的体积为19.90mL,20.00mL,均有效,标准盐酸溶液的平均体积为19.95mL, HCl~NaOH
分析,可知c(待测)偏大;所以答案是:待测溶液润洗锥形瓶;偏高;(4)根据酸式滴定管用蒸馏水洗净后,应用标准盐酸润洗,以防被稀释;所以答案是:用标准液润洗滴定管;(5)待测液的物质的量不变,读数时目光平视,凹液面最低点与刻度线相切,所以读数为22.60mL;所以答案是:22.60;(6)两次消耗的盐酸标准液的体积为19.90mL,20.00mL,均有效,标准盐酸溶液的平均体积为19.95mL, HCl~NaOH
1 1
0.1000molL﹣1×19.95mL c(NaOH)×25.00mL
解得:c(NaOH)=0.08mol/L;
所以答案是:0.08.
【考点精析】掌握酸碱中和滴定是解答本题的根本,需要知道中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准液;先用待测液润洗后在移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示, K值大小与温度的关系是:温度升高,K值 。(填一定增大、一定减小、或可能增大也可能减小)。
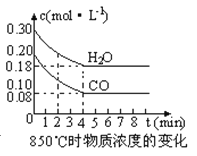
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g) +H2O(g) ![]() CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=mol·L-1·min-1。t℃时物质浓度(mol·L-1)的变化:
CO2(g) +H2 (g) △H<0,CO和H2O浓度变化如下图,则0~4min的平均反应速率v(CO)=mol·L-1·min-1。t℃时物质浓度(mol·L-1)的变化:
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min~4min之间反应处于 状态;c 1数值 0.08 mol·L-1 (填大于、小于或等于)。
②反应在4min~5min间,平衡向逆方向移动,可能的原因是 (单选),表中5min~6min之间数值发生变化,可能的原因是 (单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢俗名双氧水,医疗上利用它有杀菌消毒的作用来清洗伤口。有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:(配平和单线桥各占分数)
[ ]H2O2+[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O
(2)如消除采矿业胶液中的氰化物(如KCN,C为+2价),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,
试指出A的化学式 ,如此反应中有6.72L(标准状况)气体生成,转移电子数目为 (用NA表示)。
(3)高锰酸钾也可用于医学杀菌消毒。根据反应条件可判断氧化剂的氧化能力的强弱:例如:
MnO2+4HCl(浓)![]() MnCl2+C12↑+2H2O;
MnCl2+C12↑+2H2O;
2KMnO4+16HCl(浓)=2MnCl2+5C12↑+8H2O。
则Mn02、KMnO4氧化性 强。
某强酸反应体系中,反应物和生成物共六种物质或离子:O2、MnO4-、H2O、Mn2+、H2O2、H+。已知该反应中H2O2 只发生了如下过程:H2O2→O2.则该反应中发生还原反应的过程是:_________→_________,该反应应选择的酸是:_________(填序号)。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸
(4)用0.2 mol/L Na2SO3溶液32 mL,还原含4×10-3 mol XO42-的溶液,过量的Na2SO3用0.2mol/L KMnO4酸性溶液氧化(其中KMnO4被还原成Mn2+),共消耗KMnO4溶液0.8 mL,则元素X在还原产物中的化合价是( )
A.+1 B.+2 C.+3 D.+4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点。一种以肼(N2H4)为燃料的电池装置如图所示。该电池用空气中的氧气作为氧化剂,KOH作为电解质。下列关于该燃料电池的叙述不正确的是( )

A. 电流从右侧电极经过负载后流向左侧电极
B. 负极发生的电极反应式为N2H4+4OH--4e-===N2↑+4H2O
C. 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触
D. 该燃料电池持续放电时,K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素W、X、Y、Z的原子序数依次增大,W的原子最外层电子数是次外层电子数的3倍.X、Y和Z分属不同的周期,它们的原子序数之和是W原子序数的5倍.在由元素W、X、Y、Z组成的所有可能的二组分化合物中,由元素W与Y形成的化合物M的熔点最高.请回答下列问题:
(1)W元素原子的L层电子排布式为 , W3分子的空间构型为 .
(2)X单质与水发生主要反应的化学方程式为 .
(3)化合物M的化学式为 , 其晶体结构与NaCl相同,而熔点高于NaCl.M熔点较高的原因是 . 将一定量的化合物ZX负载在M上可制得ZX/M催化剂,用于催化碳酸二甲酯与月桂醇酯交换合成碳酸二月桂酯.在碳酸二甲酯分子中,碳原子采用的杂化方式有 , O﹣C﹣O的键角约为 .
(4)X、Y、Z可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角,Z处于体心位置,则该晶体的组成为X:Y:Z= .
(5)含有元素Z的盐的焰色反应为色.许多金属盐都可以发生焰色反应,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在四个不同的容器中,在不同条件下进行合成氨的反应,根据下列在相同时间内测定的结果判断生成氨的速率最快的是( )
A.v(H2)=0.1 mol/(Lmin)
B.v(N2)=0.1 mol/(Lmin)
C.v(N2)=0.2 mol/(Lmin)
D.v(NH3)=0.3 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL该溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加足量NaOH溶液加热后,收集到气体0.04mol。
③第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验数据,填写下列空白。
(1)一定不存在的离子有___________________。
(2)第②步操作发生反应的离子方程式为_________________________。
(3)第③步操作确定的离子有____________________________。
(4)对无法确定是否存在的离子,满足___________________时,能确定其存在。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液;②pH 试纸的使用;③过滤;④蒸发.
A. 试管 B. 胶头滴管 C. 漏斗 D. 玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学基本概念的说法不正确的是
A.乙醇和二甲醚互为同分异构体
B.碳、硫、磷均存在同素异形现象
C.氢元素存在 1H、2H、3H 三种核素,它们互为同位素
D.O2 转变成 O3 属于物理变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com