
| A. | Al$\stackrel{氧气,加热}{→}$Al2O3$\stackrel{硝酸}{→}$Al(NO3)3$\stackrel{加热蒸干}{→}$硝酸铝晶体 | |
| B. | Cu$\stackrel{氧气,加热}{→}$CuO$\stackrel{稀硫酸}{→}$CuSO4$\stackrel{蒸干结晶}{→}$胆矾 | |
| C. | Fe$\stackrel{氯气}{→}$FeCl3$\stackrel{过量氨水}{→}$Fe(OH)3$\stackrel{加热}{→}$Fe2O3 | |
| D. | FeSO4溶液$\stackrel{硫化氢、过滤}{→}$FeS |
分析 A.铝和氧气反应生成氧化铝,氧化铝和硝酸反应生成硝酸铝,硝酸铝水解生成氢氧化铝和硝酸,硝酸易挥发加热热蒸干得到水解产物氢氧化铝;
B.铜和氧气反应生成氧化铜,氧化铜和硫酸反应生成硫酸铜,硫酸铜水解生成硫酸是难挥发性酸,蒸发浓缩,冷却结晶得到晶体硫酸铜;
C.铁和氯气反应生成氯化铁,氯化铁和过量氨水反应生成氢氧化铁,加热分解得到氧化铁;
D.硫化亚铁溶于盐酸,盐酸酸性大于氢硫酸,硫酸亚铁和氢硫酸不能反应.
解答 解:A.铝和氧气反应生成氧化铝,4Al+3O2$\frac{\underline{\;\;△\;\;}}{\;}$2Al2O3,氧化铝和硝酸反应生成硝酸铝,Al2O3+6HNO3=Al(NO3)3+3H2O,硝酸铝水解生成氢氧化铝和硝酸,Al(NO3)3+3H2O?Al(OH)3+3HNO3,硝酸易挥发加热热蒸干得到水解产物氢氧化铝,不能得到硝酸铝晶体,故A错误;
B.铜和氧气反应生成氧化铜,2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,氧化铜和硫酸反应生成硫酸铜,CuO+H2SO4=CuSO4+H2O,CuSO4+H2O?Cu(OH)2+H2SO4,硫酸铜水解生成硫酸是难挥发性酸,蒸发浓缩,冷却结晶得到晶体硫酸铜,蒸干结晶得到硫酸铜,但不能得到硫酸铜晶体,故B错误;
C.铁和氯气反应生成氯化铁,2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3,氯化铁和过量氨水反应生成氢氧化铁,FeCl3+3NH3•H2O=Fe(OH)3+3NH4Cl,加热分解得到氧化铁,2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,故C正确;
D.硫化亚铁溶于盐酸,盐酸酸性大于氢硫酸,硫酸亚铁和氢硫酸不能反应,故D错误;
故选C.
点评 本题考查了物质性质、物质转化关系、盐类水解原理等知识点的理解应用,掌握基础是解题关键,题目难度中等.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:选择题
| X | ||
| Y | Z | W |
| T |
| A. | X、W、Z元素的气态氢化物的热稳定性均依次递增 | |
| B. | Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | YX2和WX3均属于离子化合物 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2Y3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 含氧酸 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
| 结构式 | Cl-OH | 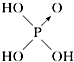 | 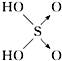 | 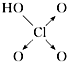 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 ,H3PO3与过量的NaOH溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O;
,H3PO3与过量的NaOH溶液反应的化学方程式为H3PO3+2NaOH=Na2HPO3+2H2O; ,在H3AsO3中加入浓盐酸,反应的化学方程式为As(OH)3+3HCl=AsCl3+3H3O.
,在H3AsO3中加入浓盐酸,反应的化学方程式为As(OH)3+3HCl=AsCl3+3H3O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳氢化合物就是烃 | |
| B. | 水、甲烷和乙烷都是10个电子的分子 | |
| C. | 乙烷的沸点比甲烷高,因而更难液化 | |
| D. | 甲烷和乙烷分子中只有一种氢,故其二氯化物也只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
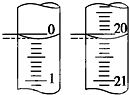 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液.
某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液.| 滴定次数 | 待测NaOH溶液的体积/mL | 0.1000mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.20 | 20.22 | |
| 第二次 | 25.00 | 0.56 | 24.54 | |
| 第三次 | 25.00 | 0.42 | 20.40 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
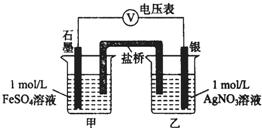 为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:
为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:| 序号 | 操作 | 现象 |
| 实验Ⅰ | 将2mL1mol/L AgNO3溶液加入到 1mL1mol/L FeSO4溶液中 | 产生白色沉淀,随后有黑色固体产生 |
| 取上层清液,滴加KSCN溶液 | 溶液变红 |
| 序号 | 操作 | 现象 |
| 实验Ⅲ | 将2mL2mol/LFe(NO3)3溶液加入有银镜的试管中 | 银镜消失 |
| 实验Ⅳ | 将2mL1mol/LFe2(SO4)3溶液加入有银镜的试管中 | 银镜减少,未消失 |
| 实验Ⅴ | 将2mL2mol/LFeCl3溶液加入有银镜的试管中 | 银镜消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢燃料电池汽车的使用可以有效减少城市空气污染 | |
| B. | 电解水制取氢气是理想而经济的制氢方法 | |
| C. | 发展氢燃料电池汽车不需要安全高效的储氢技术 | |
| D. | 氢燃料电池把氢气和氧气燃烧放出的热能转化为电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com