
(04年北京卷)(1)化合物A(![]() )是一种有机溶剂。A可以发生以下变化:
)是一种有机溶剂。A可以发生以下变化:
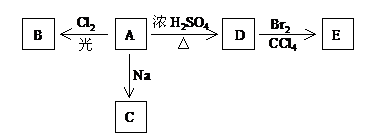
<1>A分子中的官能团名称是___________;
<2>A只有一种一氯取代物B。写出由A转化为B的化学方程式
___________________________________________________________;
<3>A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。
F的结构简式是_____________________________________________。
(2)化合物“HQ”(![]() )可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号)_______________。
)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号)_______________。
<1>加成反应 <2>氧化反应 <3>加聚反应 <4>水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是__________。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。“TBHQ”与氢氧化钠溶液作用得到化学式为![]() 的化合物。
的化合物。
“TBHQ”的结构简式是_____________________________。
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
(04年北京卷)(15分)X、Y、Z为三个不同短周期非金属元素的单质。在一定条件下有如下反应:![]() (气),
(气),![]() (气)。请针对以下两种不同情况回答:
(气)。请针对以下两种不同情况回答:
(1)若常温下X、Y、Z均为气体,且A和B化合生成固体C时有白烟产生,则:
<1>Y的化学式是_________;
<2>生成固体C的化学方程式是_______________________________________。
(2)若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
<1>B的化学式是__________;
<2>向苛性钠溶液中通入过量的A,所发生反应的离子方程式是
_____________________________________________;
<3>将Y与(1)中某单质的水溶液充分反应可生成两种强酸,该反应的化学方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(04年北京卷)(18分)资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是__________;碱石灰的作用是_______________________________。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
<1>氨催化氧化的化学方程式是___________________________________________;
试管内气体变为红棕色,该反应的化学方程式是_____________________________。
<2>停止反应后,立即关闭B中两个活塞。一段时间后,将试管浸入冰水中,试管内气体颜色变浅,请结合化学方程式说明原因_________________________________________
_____________________________________________________________________________
____________________________________________________________________________。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
<1>两气体通入的先后顺序是_______________________________________________,其理由是______________________________________________________________________
____________________________________________________________________________。
<2>氨气燃烧的化学方程式是_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(04年北京卷)用![]() 表示阿伏加德罗常数,下列叙述中正确的是()
表示阿伏加德罗常数,下列叙述中正确的是()
A. 0.1![]() 稀硫酸100mL中含有硫酸根个数为0.1
稀硫酸100mL中含有硫酸根个数为0.1![]()
B. 1mol![]() (碳正离子)中含有电子数为10
(碳正离子)中含有电子数为10![]()
C. 2.4g金属镁与足量的盐酸反应,转移电子数为2![]()
D.12.4g白磷中含有磷原子数为0.4![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
(04年北京卷)(12分)有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③。甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量。
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为________g。
(2)乙取样品②ag强热,生成的气体不能使澄清的石灰水变浑浊。再将反应后的固体与足量的稀硝酸微热,充分反应后,有bg固体剩余,该剩余固体的化学式为________。样品②中氧化铜质量为_________g(以含a、b的代数式表示)。
(3)丙称量样品③强热后剩余的固体,质量比原样品减小了cg,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com