
| A、Fe(NO3)3 |
| B、AgNO3 |
| C、Fe(NO3)2 |
| D、Mg(NO3)2 |
科目:高中化学 来源: 题型:
| A、等于1.6 mol |
| B、等于1.2 mol |
| C、大于1.6 mol |
| D、小于1.2 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
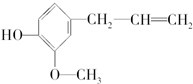 某有机物的结构简式如图,关于该物质的下列说法:①能和溴水发生取代反应 ②能发生消去反应 ③能发生氧化反应 ④能发生加成反应 ⑤能发生水解反应,其中不正确的是( )
某有机物的结构简式如图,关于该物质的下列说法:①能和溴水发生取代反应 ②能发生消去反应 ③能发生氧化反应 ④能发生加成反应 ⑤能发生水解反应,其中不正确的是( )| A、①③ | B、②⑤ | C、②③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、利用Cu(OH)2替代CuO也可调试溶液pH不影响实验结果 |
| B、若要用实验测定所得硫酸铜晶体中结晶水的数目要用到坩埚和坩埚钳 |
| C、洗涤晶体:向滤出晶体的漏斗中加少量水浸没晶体,自然流下,重复2-3次 |
| D、用18mol/L浓硫酸配制溶解所用4mol/L的稀硫酸,玻璃仪器一般只有3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ka=-Kh |
| B、Ka=Kh-1 |
| C、Ka?Kh=Kw |
| D、Ka?Kw=Kh |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v1减小,v2增大,平衡逆向移动 |
| B、v1增大,v2减小,平衡正向移动 |
| C、v1、v2同时减小,平衡逆向移动 |
| D、v1、v2同时增大,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com