
| A. | v(NH3)=0.1 mol/(L•min) | B. | v (N2)=0.6 mol/(L•min) | ||
| C. | v (N2)=0.02mol/(L•s) | D. | v (H2)=0.3 mol/(L•min) |
分析 根据化学反应速率之比等化学计量数之比进行计算,以同一个物质的化学反应速率进行比较;升高温度,加快化学反应速率.
解答 解:A.v(NH3)=0.1mol/(L•min);
B.v(H2):v(NH3)=3:2,故v(NH3)=$\frac{2}{3}$v(H2)=$\frac{2}{3}$×0.6mol/(L•min)=0.4mol/(L•min);
C.v(NH3):v(N2)=2:1,故v(NH3)=2v(N2)=2×0.02mol/(L•s)=0.04mol/(L•s)×60=2.4mol/(L•min);
D.v(H2):v(NH3)=3:2,故v(NH3)=$\frac{2}{3}$v(H2)=$\frac{2}{3}$×0.3mol/(L•min)=0.2mol/(L•min),故C的反应速率最快,故C反应所处的温度最高,
故选C.
点评 本题考查化学反应速率的相关计算以及温度对化学反应速率的影响,难度不大.要注意比较化学反应速率快慢要以同一个物质进行比较.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 0.1 mol•L-1稀硫酸中含有硫酸根个数为0.1NA | |
| B. | 常温下,1.12 L氮气所含原子数为0.1NA | |
| C. | 1 mol Na2O2与足量的盐酸反应,转移电子数为2NA | |
| D. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②③④ | C. | ①②④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{14}$C表示质子数为6、中子数为8的核素 | |
| B. | 甲醇(CH3OH)和甘油( 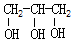 )互为同系物 )互为同系物 | |
| C. | C5H12的同分异构体有3种,其沸点各不相同 | |
| D. | CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷' |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{100ρ}{41}$ mol•L-1 | B. | $\frac{20}{ρ}$ mol•L-1 | C. | $\frac{50ρ}{41}$ mol•L-1 | D. | $\frac{25ρ}{41}$ mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com