
| 3 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
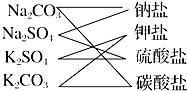 ��ͼ��ʾ�Ƕ�Na2CO3��Na2SO4��K2CO3��K2SO4�������ʽ��еķ��࣬���ַ�����������ǣ�������
��ͼ��ʾ�Ƕ�Na2CO3��Na2SO4��K2CO3��K2SO4�������ʽ��еķ��࣬���ַ�����������ǣ�������| A��������෨ | B����״���෨ |
| C��Ȧͼ�� | D����״��ͷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ЧӦ | B�������˶� |
| C����Ӿ | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
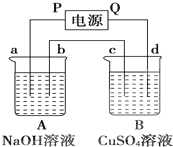 ����ͼװ��ʵ�飬A��B���ձ��ֱ�ʢ��200g10% NaOH��Һ������CuSO4��Һ��ͨ��һ��ʱ���c������Cu�������ֲ���ձ�A��Һ����������4.5g���缫��Ϊʯī�缫���Իش�
����ͼװ��ʵ�飬A��B���ձ��ֱ�ʢ��200g10% NaOH��Һ������CuSO4��Һ��ͨ��һ��ʱ���c������Cu�������ֲ���ձ�A��Һ����������4.5g���缫��Ϊʯī�缫���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ͼ��ʾװ�ý���ʵ�飬��Һ��A��μ��뵽����B�У��ش��������⣺
����ͼ��ʾװ�ý���ʵ�飬��Һ��A��μ��뵽����B�У��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com