
到目前为止,由化学能转变为热能或电能仍然是人类使用最主要的能源。
(1)化学反应中放出的热能(焓变,ΔH)与反应物和生成物在反应过程中断键和形成新键过程中吸收和放出能量的大小有关。
已知:H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1,断裂1 mol H—H键吸收的能量为436 kJ,断裂1 mol Cl—Cl键吸收的能量为247 kJ,则形成1 mol H—Cl键放出的能量为________。
(2)燃料燃烧将其所含的化学能转变为我们所需要的热能。已知:
①CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.3 kJ·mol-1
②C(s,石墨)+O2(g)===CO2(g)
ΔH=-393.5 kJ·mol- 1
1
③2H2(g)+O2(g)===2H2O(l)
ΔH=-571.6 kJ·mol-1
标准状况下22.4 L氢气和甲烷的混合气体在足量的氧气中充分燃烧反应放出588.05 kJ的热量,原混合气体中氢气的质量是________。根据以上三个热化学方程式,计算C(s,石墨)+2H2(g)===CH4(g)的反应热ΔH为________。
解析 (1)H2(g)+Cl2(g)===2HCl(g) ΔH=-185 kJ·mol-1,该反应的ΔH=旧键断裂吸收的能量-新键形成放出的能量,设形成1 mol H—Cl键放出的能量为x,则每发生这样的反应1 mol,ΔH=436 kJ·mol-1+247 kJ·mol-1-2x=-185 kJ·mol-1,解得x=434 kJ·mol-1,所以每形成1 mol H—Cl键放出434 kJ的热量。
(2)设混合气体中CH4的物质的量为a,H2的物质的量为b,a+b=1 mol,890.3 kJ·mol-1×a+571.6 kJ·mol-1×b/2=588.05 kJ,解得a=0.5 mol,b=0.5 mol,所以H2的质量为0.5 mol×2 g·mol-1=1.0 g。
根据反应C(s,石墨)+2H2(g)===CH4(g)可知,②+③-①即得,所以该反应的反应热为ΔH=-571.6 kJ·mol-1-393.5 kJ·mol-1+890.3 kJ·mol-1=-74.8 kJ·mol-1。
kJ·mol-1。
答 案 (1)434 kJ (2)1.0 g -74.8 kJ·mol-1
案 (1)434 kJ (2)1.0 g -74.8 kJ·mol-1


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知
| W | X | |
| Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性强于Y
D.Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示温度、压强对达平衡的可逆反应:2L(g)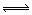 2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
2M(g)+N(g) △H>0的影响(P1<P2 ) 图中y轴表示的意义是 ( )
A.混合物中L的百分含量
B.混合气体的密度
C.L的转化率
D.混合气体的平均分子量

查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属及金属键的说法正确的是
A.金属键具有方向性与饱和性
B.金属键是金属阳离子与自由电子间的相互作用
C.金属导电是因为在外加电场作用下产生自由电子
D.金属具有光泽是因为金属阳离子吸收并放出可见光
查看答案和解析>>
科目:高中化学 来源: 题型:
根据碘与氢气反应的热化学方程式:
(ⅰ)I2(g)+H2(g)  2HI(g) ΔH=-9.48 kJ·mol-1
2HI(g) ΔH=-9.48 kJ·mol-1
(ⅱ)I2(s)+H2(g)  2HI(g) ΔH=+26.48 kJ·mol-1
2HI(g) ΔH=+26.48 kJ·mol-1
下列判断正确的是
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(ⅰ)的产物比反应(ⅱ)的产物稳定
D.反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是
mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是

A.194 B.391
C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.鸡蛋壳浸泡在盐酸中产生气泡:CO +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
B.四氧化三铁固体溶解在稀硝酸中: Fe3O4+8H+===2Fe3++Fe2++4H2O
C.将氨气通入硫酸溶液中: NH3+H+===NH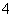
D.向碳酸氢铵溶液中加入足量的NaOH溶液: NH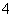 +OH-===NH3·H2O
+OH-===NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生对SO2与漂粉精的反应进行实验探究:
| 操作 | 现象 |
| 取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
|
| i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是 ________________________________。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是______________________。
(3)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成。进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
① 实验a的目的是_____________________________________________________。
②由实验a、b不能判断白雾中含有HCl,理由是________________________________。
(4)现象ii中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应。通过进一步实验确认了这种可能性,其实验方案是______________________
________________________。
(5)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是________。
②用离子方程式解释现象iii中黄绿色褪去的原因:__________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com