
 2013年12月14日,嫦娥三号顺利月面软着陆,月球车表面包裹F46膜,F46膜是由四氟乙烯和全氟丙烯共聚而成.下列有关说法正确的是( )
2013年12月14日,嫦娥三号顺利月面软着陆,月球车表面包裹F46膜,F46膜是由四氟乙烯和全氟丙烯共聚而成.下列有关说法正确的是( )| A、F46膜是纯净物 |
| B、全氟丙烯属于有机物 |
| C、全氟丙烯所有原子共平面 |
| D、四氟乙烯分子中只含非极性键 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
 (1)与N元素同周期的第一电离能最大且电负性最小的元素的基态原子核外电子排布式为
(1)与N元素同周期的第一电离能最大且电负性最小的元素的基态原子核外电子排布式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可加入硫酸以提高电解质的导电性 |
| B、充电时LiFePO4只发生还原反应 |
| C、充电过程中,电池正极材料的质量增大 |
| D、放电时电池正极反应为:FePO4+Li++e-═LiFePO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-4akJ?mol-1 | ||
B、C2H2(g)+
| ||
| C、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2akJ?mol-1 | ||
| D、2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=akJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
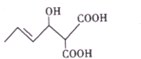
| A、其分子式为C7H10O5 |
| B、分子中含有三种官能团 |
| C、1mol该物质能与3mol NaOH溶液反应 |
| D、能使溴的四氯化碳溶液或酸性高猛酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原料苯酚能和NaHCO3溶液反应 |
| B、菠萝酯可以使溴水、高锰酸钾溶液褪色 |
| C、中间体中所有的原子都可以共平面 |
| D、中间体和菠萝酯中均不含手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
2- 7 |
2- 4 |
2- 7 |
2- 7 |
| A、①② | B、①③ | C、①④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、最外层电子数为2的元素一定处于ⅡA族 |
| B、Ba(OH)2是离子化合物,既含离子键又含共价键 |
| C、Na的原子半径比Cl的大,但Na+的半径比Cl-的小 |
| D、Cl与Ⅰ同属ⅦA族元素,两者最高价氧化物对应水化物的酸性HClO4>HIO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com