
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,且K、M层电子数之和等于L层电子数 |
| B | 最外层电子数是次外层电的2倍 |
| C | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
 .
.分析 短周期元素中,A元素原子有三个电子层,且K、M层电子数之和等于L层电子数,则M层电子数为8-2=6,故A为S元素;B元素原子最外层电子数是次外层电的2倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;常温下C的单质为双原子分子,其氢化物的水溶液呈碱性,则C为N元素;D元素最高正价是+7价,则D为Cl,以此解答该题.
解答 解:短周期元素中,A元素原子有三个电子层,且K、M层电子数之和等于L层电子数,则M层电子数为8-2=6,故A为S元素;B元素原子最外层电子数是次外层电的2倍,原子只能有2个电子层,最外层电子数为4,故B为碳元素;常温下C的单质为双原子分子,其氢化物的水溶液呈碱性,则C为N元素;D元素最高正价是+7价,则D为Cl.
(1)A为S元素,在周期表中的位置:第三周期第ⅥA族,
故答案为:第三周期第ⅥA族;
(2)C元素的单质为N2,电子式为 ,故答案为:
,故答案为: ;
;
(3)同周期自左而右非金属性增强,故非金属性Cl>S;
a.物质的状态属于物理性质,不能判断非金属性强弱,故错误;
b.元素氢化物稳定性与元素非金属性一致,D(氯)的氢化物比A(硫)的氢化物稳定,说明D非金属性故A强,故正确;
c.非金属单质与金属与变价金属反应,根据生成物中变价金属化合价可以判断非金属元素的非金属性强弱,但Na不是变价金属,故错误,
故答案为:Cl;b;
(4)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物 的水化物分别为硫酸、碳酸、硝酸、高氯酸,其中碳酸为弱酸,其它三种为强弱,故化学性质明显不同于其他三种的是 H2CO3,
故答案为:H2CO3.
点评 本题考查结构性质位置关系应用,为高考常见题型,侧重于学生的分析能力的考查,推断元素是解题关键,注意金属性、非金属性强弱比较实验事实,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Na2O2 既是氧化剂,又是还原剂 | |
| B. | Fe2O3在反应中得到电子 | |
| C. | 3 mol Na2O2参加反应,转移的电子总数为12mol | |
| D. | Na2FeO4能消毒杀菌,因其具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
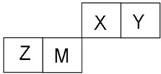 X、Y、Z、W四种短周期元素在周期表中的位置如右图,其中只有Z为金属元素.回答下列问题:
X、Y、Z、W四种短周期元素在周期表中的位置如右图,其中只有Z为金属元素.回答下列问题: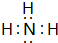 ,该气态氢化物可以用浓盐酸来检验,其反应产物的化学式为NH4Cl,所得产物中包含的化学键为离子键、共价键.
,该气态氢化物可以用浓盐酸来检验,其反应产物的化学式为NH4Cl,所得产物中包含的化学键为离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应速率等于逆反应速率 | B. | 各组分浓度不再发生变化 | ||
| C. | 反应体系中某组分的组成保持不变 | D. | 正、逆反应速率都为零 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
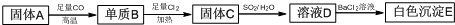
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
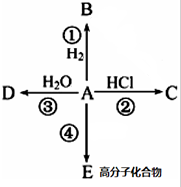 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下课发生如图所示的转化,请回答下列问题.
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下课发生如图所示的转化,请回答下列问题.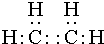 ,D中所含的官能团为羟基.
,D中所含的官能团为羟基.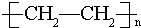 ,反应类型为加聚反应.
,反应类型为加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测定新制氯水的pH=2 | |
| B. | 用玻璃棒在过滤器上搅拌以加速硫酸铜晶体的洗涤 | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则该溶液中不一定含有SO${\;}_{4}^{2-}$ | |
| D. | 向可溶性淀粉溶液中滴加碘酒,溶液呈蓝色,用CCl4作萃取剂振荡、静置后,下层呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
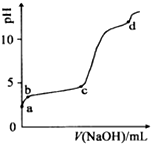
| A. | a点溶液呈酸性的原因是Al3+水解,离子方程为:Al3++3OH-?Al(OH)3 | |
| B. | c点铝元素主要以Al(OH)3的形式存在 | |
| C. | a-b段,溶液pH增大,Al3+浓度不变 | |
| D. | d点Al(OH)3沉淀开始溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com